એમિનો એસિડ એ કોઈપણ જીવંત જીવની મુખ્ય નિર્માણ સામગ્રી છે. તેમની પ્રકૃતિ દ્વારા, તેઓ છોડના પ્રાથમિક નાઇટ્રોજનયુક્ત પદાર્થો છે, જે જમીનમાંથી સંશ્લેષણ કરવામાં આવે છે. એમિનો એસિડની રચના તેમની રચના પર આધારિત છે.
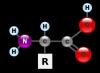
એમિનો એસિડ માળખું
તેના દરેક પરમાણુમાં કાર્બોક્સિલ અને એમાઈન જૂથો હોય છે, જે રેડિકલ સાથે જોડાયેલા હોય છે. જો એમિનો એસિડમાં 1 કાર્બોક્સિલ અને 1 એમિનો જૂથ હોય, તો તેની રચના નીચે પ્રસ્તુત સૂત્ર દ્વારા સૂચવી શકાય છે.

એમિનો એસિડ કે જેમાં 1 એસિડ અને 1 આલ્કલાઇન જૂથ હોય છે તેને મોનોએમિનોમોનોકાર્બોક્સિલિક એસિડ કહેવામાં આવે છે. સજીવોમાં, 2 કાર્બોક્સિલ જૂથો અથવા 2 એમાઈન જૂથો પણ સંશ્લેષણ કરવામાં આવે છે અને જેનાં કાર્યો નક્કી કરવામાં આવે છે. 2 કાર્બોક્સિલ અને 1 એમાઈન જૂથો ધરાવતા એમિનો એસિડને મોનોએમિનોડિકાર્બોક્સિલિક કહેવામાં આવે છે, અને જે 2 એમાઈન અને 1 કાર્બોક્સિલ ધરાવે છે તેને ડાયમિનોમોનોકાર્બોક્સિલિક કહેવામાં આવે છે.
તેઓ ઓર્ગેનિક રેડિકલ R ની રચનામાં પણ ભિન્ન છે. તેમાંના દરેકનું પોતાનું નામ અને માળખું છે. તેથી એમિનો એસિડના વિવિધ કાર્યો. તે એસિડિક અને આલ્કલાઇન જૂથોની હાજરી છે જે તેની ઉચ્ચ પ્રતિક્રિયાશીલતાને સુનિશ્ચિત કરે છે. આ જૂથો એમિનો એસિડને જોડે છે અને પોલિમર - પ્રોટીન બનાવે છે. પ્રોટીનને તેમની રચનાને કારણે પોલીપેપ્ટાઈડ્સ પણ કહેવામાં આવે છે.
મકાન સામગ્રી તરીકે એમિનો એસિડ
પ્રોટીન પરમાણુ એ દસ અથવા સેંકડો એમિનો એસિડની સાંકળ છે. પ્રોટીન્સ એમિનો એસિડની રચના, જથ્થા અને ક્રમમાં અલગ પડે છે, કારણ કે 20 ઘટકોના સંયોજનોની સંખ્યા લગભગ અનંત છે. તેમાંના કેટલાકમાં આવશ્યક એમિનો એસિડની સંપૂર્ણ રચના હોય છે, અન્ય એક અથવા વધુ વિના કરે છે. વ્યક્તિગત એમિનો એસિડ, એક માળખું કે જેના કાર્યો માનવ શરીરના પ્રોટીન જેવા જ હોય છે, તેનો ખોરાક ઉત્પાદનો તરીકે ઉપયોગ થતો નથી, કારણ કે તે નબળી રીતે દ્રાવ્ય હોય છે અને જઠરાંત્રિય માર્ગ દ્વારા વિભાજિત થતા નથી. તેમાં નખ, વાળ, ફર અથવા પીછાના પ્રોટીનનો સમાવેશ થાય છે.
એમિનો એસિડના કાર્યોને વધુ પડતો અંદાજ કાઢવો મુશ્કેલ છે. આ પદાર્થો માનવ આહારમાં મુખ્ય ખોરાક છે. એમિનો એસિડ શું કાર્ય કરે છે? તેઓ સ્નાયુ સમૂહની વૃદ્ધિમાં વધારો કરે છે, સાંધા અને અસ્થિબંધનને મજબૂત કરવામાં મદદ કરે છે, શરીરના ક્ષતિગ્રસ્ત પેશીઓને પુનઃસ્થાપિત કરે છે અને માનવ શરીરમાં થતી તમામ પ્રક્રિયાઓમાં ભાગ લે છે.

આવશ્યક એમિનો એસિડ
ફક્ત પૂરક અથવા ખાદ્ય ઉત્પાદનોમાંથી જ તમે તંદુરસ્ત સાંધાઓ બનાવવાની પ્રક્રિયામાં કાર્યો મેળવી શકો છો, મજબૂત સ્નાયુઓ, સુંદર વાળ ખૂબ જ મહત્વપૂર્ણ છે. આ એમિનો એસિડમાં શામેલ છે:
- ફેનીલાલેનાઇન;
- લાયસિન;
- થ્રેઓનાઇન;
- methionine;
- વેલિન
- leucine;
- ટ્રિપ્ટોફન;
- હિસ્ટિડિન;
- આઇસોલ્યુસિન
આવશ્યક એમિનો એસિડના કાર્યો
આ ઇંટો માનવ શરીરના દરેક કોષની કામગીરીમાં આવશ્યક કાર્યો કરે છે. જ્યાં સુધી તેઓ શરીરમાં પૂરતી માત્રામાં પ્રવેશ કરે ત્યાં સુધી તેઓ અદ્રશ્ય હોય છે, પરંતુ તેમની ઉણપ સમગ્ર શરીરની કામગીરીને નોંધપાત્ર રીતે નબળી પાડે છે.
- વેલિન સ્નાયુઓને નવીકરણ કરે છે અને ઊર્જાના ઉત્તમ સ્ત્રોત તરીકે સેવા આપે છે.
- હિસ્ટીડિન લોહીની રચનામાં સુધારો કરે છે, સ્નાયુઓની પુનઃપ્રાપ્તિ અને વૃદ્ધિને પ્રોત્સાહન આપે છે અને સંયુક્ત કાર્યમાં સુધારો કરે છે.
- આઇસોલ્યુસિન હિમોગ્લોબિનનું ઉત્પાદન કરવામાં મદદ કરે છે. લોહીમાં ખાંડની માત્રાને નિયંત્રિત કરે છે, વ્યક્તિની શક્તિ અને સહનશક્તિ વધારે છે.
- લ્યુસીન રોગપ્રતિકારક શક્તિને મજબૂત બનાવે છે, લોહીમાં ખાંડ અને લ્યુકોસાઈટ્સના સ્તરને મોનિટર કરે છે. જો લ્યુકોસાઈટ્સનું સ્તર ખૂબ ઊંચું હોય: તે તેમને ઘટાડે છે અને બળતરા દૂર કરવા માટે શરીરના અનામતને સક્રિય કરે છે.
- લાયસિન કેલ્શિયમને શોષવામાં મદદ કરે છે, જે હાડકાંનું નિર્માણ અને મજબૂતીકરણ કરે છે. કોલેજન ઉત્પાદનમાં મદદ કરે છે, વાળનું માળખું સુધારે છે. પુરુષો માટે, આ એક ઉત્તમ એનાબોલિક સ્ટીરોઈડ છે, કારણ કે તે સ્નાયુઓ બનાવે છે અને પુરુષ શક્તિ વધારે છે.
- મેથિઓનાઇન પાચન તંત્ર અને યકૃતની કામગીરીને સામાન્ય બનાવે છે. ચરબીના ભંગાણમાં ભાગ લે છે, સગર્ભા સ્ત્રીઓમાં ટોક્સિકોસિસ દૂર કરે છે અને વાળ પર ફાયદાકારક અસર કરે છે.
- થ્રેઓનિન જઠરાંત્રિય માર્ગની કામગીરીમાં સુધારો કરે છે. રોગપ્રતિકારક શક્તિ વધે છે, ઇલાસ્ટિન અને કોલેજનના નિર્માણમાં ભાગ લે છે. થ્રેઓનિન લીવરમાં ચરબી જમા થતા અટકાવે છે.
- ટ્રિપ્ટોફન માનવ લાગણીઓ માટે જવાબદાર છે. સેરોટોનિન ઉત્પન્ન કરે છે - સુખનું હોર્મોન, જેનાથી ઊંઘ સામાન્ય થાય છે અને મૂડ વધે છે. ટેમ્સ ભૂખ, હૃદયના સ્નાયુઓ અને ધમનીઓ પર ફાયદાકારક અસર કરે છે.
- ફેનીલાલેનાઇન ચેતા કોષોથી માથાના મગજમાં સિગ્નલના ટ્રાન્સમીટર તરીકે કામ કરે છે. મૂડ સુધારે છે, બિનઆરોગ્યપ્રદ ભૂખને દબાવી દે છે, મેમરી સુધારે છે, સંવેદનશીલતા વધારે છે, પીડા ઘટાડે છે.
આવશ્યક એમિનો એસિડની ઉણપથી વૃદ્ધિ અટકી જાય છે, મેટાબોલિક ડિસઓર્ડર થાય છે અને સ્નાયુ સમૂહમાં ઘટાડો થાય છે.

બિનજરૂરી એમિનો એસિડ
આ એમિનો એસિડ છે, જેનું બંધારણ અને કાર્યો શરીરમાં ઉત્પન્ન થાય છે:
- આર્જિનિન;
- એલનાઇન
- શતાવરીનો છોડ;
- ગ્લાયસીન;
- પ્રોલાઇન;
- ટૌરીન
- ટાયરોસિન;
- ગ્લુટામેટ;
- સેરીન
- ગ્લુટામાઇન;
- ઓર્નિથિન;
- સિસ્ટીન;
- કાર્નેટીન
બિનજરૂરી એમિનો એસિડના કાર્યો
- સિસ્ટીન ઝેરી પદાર્થોને દૂર કરે છે, ત્વચા અને સ્નાયુ પેશીના નિર્માણમાં ભાગ લે છે અને કુદરતી એન્ટીઑકિસડન્ટ છે.
- ટાયરોસિન શારીરિક થાક ઘટાડે છે, ચયાપચયને વેગ આપે છે, તાણ અને હતાશા દૂર કરે છે.
- એલનાઇન સ્નાયુઓની વૃદ્ધિ માટે સેવા આપે છે અને તે ઊર્જાનો સ્ત્રોત છે.
- મેટાબોલિઝમ વધારે છે અને ભારે કસરત દરમિયાન એમોનિયાની રચના ઘટાડે છે.
- જ્યારે અસ્થિબંધન અને સાંધાઓને ઇજા થાય છે ત્યારે સિસ્ટીન પીડાને દૂર કરે છે.
- મગજની પ્રવૃત્તિ માટે જવાબદાર, લાંબા સમય સુધી શારીરિક પ્રવૃત્તિ દરમિયાન તે ગ્લુકોઝમાં ફેરવાય છે, ઊર્જા ઉત્પન્ન કરે છે.
- ગ્લુટામાઇન સ્નાયુઓને પુનઃસ્થાપિત કરે છે, રોગપ્રતિકારક શક્તિમાં સુધારો કરે છે, ચયાપચયને વેગ આપે છે, મગજના કાર્યને વધારે છે અને વૃદ્ધિ હોર્મોન બનાવે છે.
- ગ્લાયસીન સ્નાયુઓના કાર્ય, ચરબીના ભંગાણ, બ્લડ પ્રેશર અને બ્લડ સુગરને સ્થિર કરવા માટે જરૂરી છે.
- કાર્નેટીન ફેટી એસિડને કોષોમાં ખસેડે છે, જ્યાં તેઓ ઉર્જા છોડવા માટે તૂટી જાય છે, પરિણામે વધારાની ચરબી બળી જાય છે અને ઊર્જા ઉત્પન્ન થાય છે.
- ઓર્નિથિન વૃદ્ધિ હોર્મોન ઉત્પન્ન કરે છે, પેશાબની રચનાની પ્રક્રિયામાં સામેલ છે, ફેટી એસિડને તોડે છે અને ઇન્સ્યુલિન ઉત્પન્ન કરવામાં મદદ કરે છે.
- પ્રોલાઇન કોલેજનનું ઉત્પાદન સુનિશ્ચિત કરે છે, તે અસ્થિબંધન અને સાંધા માટે જરૂરી છે.
- સેરીન રોગપ્રતિકારક શક્તિમાં સુધારો કરે છે અને ઉર્જા ઉત્પન્ન કરે છે, તે ફેટી એસિડના ઝડપી ચયાપચય અને સ્નાયુઓની વૃદ્ધિ માટે જરૂરી છે.
- ટૌરિન ચરબીને તોડે છે, શરીરની પ્રતિકાર વધારે છે અને પિત્ત ક્ષારનું સંશ્લેષણ કરે છે.
પ્રોટીન અને તેના ગુણધર્મો
પ્રોટીન, અથવા પ્રોટીન, નાઇટ્રોજન ધરાવતા ઉચ્ચ-પરમાણુ સંયોજનો છે. "પ્રોટીન" ની વિભાવના, સૌપ્રથમ 1838 માં બર્ઝેલિયસ દ્વારા નિયુક્ત, ગ્રીક શબ્દ પરથી આવે છે અને તેનો અર્થ "પ્રાથમિક" થાય છે, જે પ્રકૃતિમાં પ્રોટીનની અગ્રણી ભૂમિકાને પ્રતિબિંબિત કરે છે. પ્રોટીનની વિવિધતા મોટી સંખ્યામાં જીવંત પ્રાણીઓનું અસ્તિત્વ શક્ય બનાવે છે: બેક્ટેરિયાથી માનવ શરીર સુધી. તેમાંના અન્ય મેક્રોમોલેક્યુલ્સ કરતાં નોંધપાત્ર રીતે વધુ છે, કારણ કે પ્રોટીન એ જીવંત કોષનો પાયો છે. તેઓ માનવ શરીરના આશરે 20% સમૂહ બનાવે છે, કોષના શુષ્ક સમૂહના 50% કરતા વધુ. વિવિધ પ્રોટીનની આ સંખ્યાને વીસ અલગ અલગ એમિનો એસિડના ગુણધર્મો દ્વારા સમજાવવામાં આવે છે, જે એકબીજા સાથે ક્રિયાપ્રતિક્રિયા કરે છે અને પોલિમર પરમાણુઓ બનાવે છે.

પ્રોટીનની ઉત્કૃષ્ટ મિલકત એ ચોક્કસ પ્રોટીનની લાક્ષણિકતા ચોક્કસ અવકાશી માળખું સ્વતંત્ર રીતે બનાવવાની ક્ષમતા છે. પ્રોટીન પેપ્ટાઈડ બોન્ડ સાથે બાયોપોલિમર્સ છે. પ્રોટીનની રાસાયણિક રચના લગભગ 16% ની સતત સરેરાશ નાઇટ્રોજન સામગ્રી દ્વારા વર્ગીકૃત થયેલ છે.
જીવન, તેમજ શરીરની વૃદ્ધિ અને વિકાસ, નવા કોષો બનાવવા માટે પ્રોટીન એમિનો એસિડના કાર્ય વિના અશક્ય છે. પ્રોટીનને અન્ય તત્વો દ્વારા બદલી શકાતા નથી; માનવ શરીરમાં તેમની ભૂમિકા અત્યંત મહત્વપૂર્ણ છે.
પ્રોટીનનાં કાર્યો
પ્રોટીનની જરૂરિયાત નીચેના કાર્યોમાં રહે છે:
- તે વૃદ્ધિ અને વિકાસ માટે જરૂરી છે, કારણ કે તે નવા કોષોના નિર્માણ માટે મુખ્ય મકાન સામગ્રી છે;
- ચયાપચયને નિયંત્રિત કરે છે, જે દરમિયાન ઊર્જા મુક્ત થાય છે. ખોરાક ખાધા પછી, ચયાપચયનો દર વધે છે, ઉદાહરણ તરીકે, જો ખોરાકમાં કાર્બોહાઇડ્રેટ્સ હોય, તો ચયાપચય 4% દ્વારા વેગ આપે છે, જો તેમાં પ્રોટીન હોય તો - 30% દ્વારા;
- તેની હાઇડ્રોફિલિસિટીને કારણે શરીરમાં નિયમન કરો - પાણીને આકર્ષવાની ક્ષમતા;
- એન્ટિબોડીઝનું સંશ્લેષણ કરીને રોગપ્રતિકારક શક્તિને મજબૂત કરો જે ચેપ સામે રક્ષણ આપે છે અને રોગના જોખમને દૂર કરે છે.

ઉત્પાદનો - પ્રોટીનના સ્ત્રોત
માનવ સ્નાયુઓ અને હાડપિંજરમાં જીવંત પેશીઓનો સમાવેશ થાય છે જે માત્ર કાર્ય જ નહીં પરંતુ સમગ્ર જીવન દરમિયાન નવીકરણ પણ કરે છે. તેઓ નુકસાનમાંથી પુનઃપ્રાપ્ત થાય છે અને તેમની શક્તિ અને ટકાઉપણું જાળવી રાખે છે. આ કરવા માટે, તેમને ખૂબ ચોક્કસ પોષક તત્વોની જરૂર છે. ખોરાક શરીરને બધી પ્રક્રિયાઓ માટે જરૂરી ઊર્જા પૂરી પાડે છે, જેમાં સ્નાયુઓની કામગીરી, પેશીઓની વૃદ્ધિ અને સમારકામનો સમાવેશ થાય છે. અને શરીરમાં પ્રોટીનનો ઉપયોગ ઊર્જાના સ્ત્રોત તરીકે અને મકાન સામગ્રી તરીકે થાય છે.

તેથી, ખોરાકમાં તેનો દૈનિક ઉપયોગ અવલોકન કરવું ખૂબ જ મહત્વપૂર્ણ છે. પ્રોટીનયુક્ત ખોરાક: ચિકન, ટર્કી, લીન હેમ, ડુક્કરનું માંસ, બીફ, માછલી, ઝીંગા, કઠોળ, દાળ, બેકન, ઇંડા, બદામ. આ તમામ ઉત્પાદનો શરીરને પ્રોટીન પ્રદાન કરે છે અને જીવન માટે જરૂરી ઊર્જા પૂરી પાડે છે.
1.એમિનો એસિડનું પ્રદર્શન એમ્ફોટેરિક ગુણધર્મોઅને એસિડ અને એમાઇન્સ, તેમજ આ જૂથોની સંયુક્ત હાજરીને કારણે ચોક્કસ ગુણધર્મો. જલીય દ્રાવણમાં, AMK આંતરિક ક્ષાર (દ્વિધ્રુવી આયનો) સ્વરૂપે અસ્તિત્વ ધરાવે છે. મોનોએમિનોમોનોકાર્બોક્સિલિક એસિડના જલીય દ્રાવણો લિટમસ માટે તટસ્થ હોય છે, કારણ કે તેમના પરમાણુઓમાં સમાન સંખ્યામાં -NH 2 - અને -COOH જૂથો હોય છે. આ જૂથો આંતરિક ક્ષાર બનાવવા માટે એકબીજા સાથે ક્રિયાપ્રતિક્રિયા કરે છે:
આવા પરમાણુમાં બે જગ્યાએ વિરોધી શુલ્ક હોય છે: હકારાત્મક NH 3 + અને કાર્બોક્સિલ –COO - પર નકારાત્મક. આ સંદર્ભમાં, એએમકેના આંતરિક મીઠાને બાયપોલર આયન અથવા ઝ્વિટર આયન (ઝ્વિટર - હાઇબ્રિડ) કહેવામાં આવે છે.
એસિડિક વાતાવરણમાં દ્વિધ્રુવી આયન કેશનની જેમ વર્તે છે, કારણ કે કાર્બોક્સિલ જૂથના વિયોજનને દબાવવામાં આવે છે; આલ્કલાઇન વાતાવરણમાં - એક આયન તરીકે. દરેક એમિનો એસિડ માટે વિશિષ્ટ pH મૂલ્યો હોય છે, જેમાં દ્રાવણમાં એનિઓનિક સ્વરૂપોની સંખ્યા cationic સ્વરૂપોની સંખ્યા જેટલી હોય છે. pH મૂલ્ય કે જેના પર AMK પરમાણુનો કુલ ચાર્જ 0 છે તેને AMK (pI AA) નો આઇસોઇલેક્ટ્રિક બિંદુ કહેવામાં આવે છે.
મોનોએમિનોડિકાર્બોક્સિલિક એસિડના જલીય દ્રાવણમાં એસિડિક પ્રતિક્રિયા હોય છે:
HOOC-CH 2 -CH-COOH « - OOC-CH 2 -CH–COO - + H +
મોનોએમિનોડિકાર્બોક્સિલિક એસિડનું આઇસોઇલેક્ટ્રિક બિંદુ એસિડિક વાતાવરણમાં છે અને આવા AMA ને એસિડિક કહેવામાં આવે છે.
ડાયમિનોમોનોકાર્બોક્સિલિક એસિડ જલીય દ્રાવણમાં મૂળભૂત ગુણધર્મો ધરાવે છે (વિયોજન પ્રક્રિયામાં પાણીની ભાગીદારી દર્શાવવી આવશ્યક છે):
NH 2 -(CH 2) 4 -CH-COOH + H 2 O « NH 3 + -(CH 2) 4 -CH–COO - + OH -
ડાયામિનોમોનોકાર્બોક્સિલિક એસિડનું આઇસોઇલેક્ટ્રિક બિંદુ pH>7 પર છે અને આવા AMA ને મૂળભૂત કહેવામાં આવે છે.
દ્વિધ્રુવી આયનો હોવાને કારણે, એમિનો એસિડ એમ્ફોટેરિક ગુણધર્મો દર્શાવે છે: તેઓ એસિડ અને પાયા બંને સાથે ક્ષાર રચવામાં સક્ષમ છે:
હાઇડ્રોક્લોરિક એસિડ HCl સાથેની ક્રિયાપ્રતિક્રિયા મીઠાની રચના તરફ દોરી જાય છે:
R-CH-COOH + HCl ® R-CH-COOH
NH 2 NH 3 + Cl -
આધાર સાથેની ક્રિયાપ્રતિક્રિયા મીઠાની રચના તરફ દોરી જાય છે:
R-CH(NH 2)-COOH + NaOH ® R-CH(NH 2)-COONa + H 2 O
2. ધાતુઓ સાથે સંકુલની રચના- ચેલેટ સંકુલ. ગ્લાયકોલ (ગ્લાયસીન) ના કોપર સોલ્ટની રચના નીચેના સૂત્ર દ્વારા રજૂ કરી શકાય છે:

માનવ શરીરમાં ઉપલબ્ધ લગભગ તમામ તાંબુ (100 મિલિગ્રામ) આ સ્થિર પંજા-આકારના સંયોજનોના સ્વરૂપમાં પ્રોટીન (એમિનો એસિડ) સાથે બંધાયેલ છે.
3. અન્ય એસિડની જેમ એમિનો એસિડ એસ્ટર, હેલોજન એનહાઇડ્રાઇડ્સ, એમાઇડ્સ બનાવે છે.
4. ડેકાર્બોક્સિલેશન પ્રતિક્રિયાઓખાસ ડેકાર્બોક્સિલેઝ એન્ઝાઇમ્સની ભાગીદારી સાથે શરીરમાં થાય છે: પરિણામી એમાઇન્સ (ટ્રિપ્ટામાઇન, હિસ્ટામાઇન, સેરોટીનાઇન) ને બાયોજેનિક એમાઇન્સ કહેવામાં આવે છે અને તે માનવ શરીરના સંખ્યાબંધ શારીરિક કાર્યોના નિયમનકાર છે.
5. ફોર્માલ્ડિહાઇડ સાથે ક્રિયાપ્રતિક્રિયા(એલ્ડીહાઇડ્સ)
R-CH-COOH + H 2 C=O ® R-CH-COOH
ફોર્માલ્ડિહાઇડ NH 2 જૂથને બાંધે છે, -COOH જૂથ મુક્ત રહે છે અને આલ્કલી સાથે ટાઇટ્રેટ કરી શકાય છે. તેથી, આ પ્રતિક્રિયાનો ઉપયોગ એમિનો એસિડ (Sørensen પદ્ધતિ) ના જથ્થાત્મક નિર્ધારણ માટે થાય છે.
6. નાઈટ્રસ એસિડ સાથે ક્રિયાપ્રતિક્રિયાહાઇડ્રોક્સી એસિડની રચના અને નાઇટ્રોજનના પ્રકાશન તરફ દોરી જાય છે. પ્રકાશિત નાઇટ્રોજન N2 ના વોલ્યુમના આધારે, અભ્યાસ હેઠળના ઑબ્જેક્ટમાં તેની માત્રાત્મક સામગ્રી નક્કી કરવામાં આવે છે. આ પ્રતિક્રિયાનો ઉપયોગ એમિનો એસિડના જથ્થાત્મક નિર્ધારણ માટે થાય છે (વેન-સ્લાઈક પદ્ધતિ):
R-CH-COOH + HNO 2 ® R-CH-COOH + N 2 + H 2 O
શરીરની બહાર AMK ને ડિમિનેટ કરવાની આ એક રીત છે
7. એમિનો એસિડનું એસિલેશન. AMK ના એમિનો જૂથને પહેલાથી જ ઓરડાના તાપમાને એસિડ ક્લોરાઇડ્સ અને એનહાઇડ્રાઇડ્સ સાથે એસીલેટેડ કરી શકાય છે.
નોંધાયેલ પ્રતિક્રિયાનું ઉત્પાદન એસીટીલ-α-એમિનોપ્રોપિયોનિક એસિડ છે.
એએમકેના એસિલ ડેરિવેટિવ્સનો વ્યાપકપણે પ્રોટીનમાં તેમના ક્રમનો અભ્યાસ કરવા અને પેપ્ટાઈડ્સના સંશ્લેષણમાં (એમિનો જૂથનું રક્ષણ) ઉપયોગ થાય છે.
8.વિશિષ્ટ ગુણધર્મોએમિનો અને કાર્બોક્સિલ જૂથોની હાજરી અને પરસ્પર પ્રભાવ સાથે સંકળાયેલ પ્રતિક્રિયાઓ - પેપ્ટાઇડ્સની રચના. a-AMK ની સામાન્ય મિલકત છે પોલી કન્ડેન્સેશન પ્રક્રિયા, પેપ્ટાઇડ્સની રચના તરફ દોરી જાય છે. આ પ્રતિક્રિયાના પરિણામે, એક એએમકેના કાર્બોક્સિલ જૂથ અને બીજા એએમકેના એમિનો જૂથ વચ્ચે ક્રિયાપ્રતિક્રિયાના સ્થળે એમાઈડ બોન્ડ રચાય છે. બીજા શબ્દોમાં કહીએ તો, પેપ્ટાઇડ્સ એમિનો જૂથો અને એમિનો એસિડના કાર્બોક્સિલ્સની ક્રિયાપ્રતિક્રિયાના પરિણામે રચાયેલી એમાઇડ્સ છે. આવા સંયોજનોમાંના એમાઈડ બોન્ડને પેપ્ટાઈડ બોન્ડ કહેવામાં આવે છે (પેપ્ટાઈડ જૂથ અને પેપ્ટાઈડ બોન્ડનું માળખું સમજાવો: થ્રી-સેન્ટર p, p-સંયોજિત સિસ્ટમ)
પરમાણુમાં એમિનો એસિડ અવશેષોની સંખ્યાના આધારે, di-, tri-, tetrapeptides, વગેરેને અલગ પાડવામાં આવે છે. પોલિપેપ્ટાઇડ્સ સુધી (100 AMK અવશેષો સુધી). ઓલિગોપેપ્ટાઇડ્સમાં 2 થી 10 AMK અવશેષો હોય છે, પ્રોટીનમાં 100 થી વધુ AMK અવશેષો હોય છે, સામાન્ય રીતે, એક પોલિપેપ્ટાઇડ સાંકળ આકૃતિ દ્વારા રજૂ કરી શકાય છે:
H 2 N-CH-CO-NH-CH-CO-NH-CH-CO-... -NH-CH-COOH
જ્યાં R 1, R 2, ... R n એ એમિનો એસિડ રેડિકલ છે.
પ્રોટીનનો ખ્યાલ.
એમિનો એસિડના સૌથી મહત્વપૂર્ણ બાયોપોલિમર્સ પ્રોટીન છે - પ્રોટીન. માનવ શરીરમાં લગભગ 5 મિલિયન છે. વિવિધ પ્રોટીન કે જે ત્વચા, સ્નાયુઓ, રક્ત અને અન્ય પેશીઓ બનાવે છે. પ્રોટીન્સ (પ્રોટીન) ને તેમનું નામ ગ્રીક શબ્દ "પ્રોટોસ" પરથી મળે છે - પ્રથમ, સૌથી મહત્વપૂર્ણ. પ્રોટીન શરીરમાં સંખ્યાબંધ મહત્વપૂર્ણ કાર્યો કરે છે: 1. બાંધકામ કાર્ય; 2. પરિવહન કાર્ય; 3. રક્ષણાત્મક કાર્ય; 4. ઉત્પ્રેરક કાર્ય; 5. હોર્મોનલ કાર્ય; 6. પોષક કાર્ય.
બધા કુદરતી પ્રોટીન એમિનો એસિડ મોનોમર્સમાંથી રચાય છે. જ્યારે પ્રોટીનનું હાઇડ્રોલાઇઝ્ડ થાય છે, ત્યારે એએમકેનું મિશ્રણ રચાય છે. આમાંથી 20 AMK છે.
4. ચિત્રાત્મક સામગ્રી:રજૂઆત
5. સાહિત્ય:
મુખ્ય સાહિત્ય:
1. બાયોઓર્ગેનિક કેમિસ્ટ્રી: પાઠ્યપુસ્તક. ટ્યુકાવકીના એન.એ., બૌકોવ યુ.આઈ. 2014
- Seitembetov T.S. રસાયણશાસ્ત્ર: પાઠ્યપુસ્તક - અલ્માટી: EVERO LLP, 2010. - 284 પૃષ્ઠ.
- બોલિસ્બેકોવા એસ.એમ. બાયોજેનિક તત્વોનું રસાયણશાસ્ત્ર: પાઠ્યપુસ્તક - સેમી, 2012. - 219 પૃષ્ઠ. : કાંપ
- વેરેન્ટોવા એલ.જી. અકાર્બનિક, ભૌતિક અને કોલોઇડલ રસાયણશાસ્ત્ર: પાઠ્યપુસ્તક - અલ્માટી: એવેરો, 2009. - 214 પૃષ્ઠ. : બીમાર.
- ભૌતિક અને કોલોઇડલ રસાયણશાસ્ત્ર / એ.પી. બેલિયાએવ દ્વારા સંપાદિત - એમ.: જીઓટાર મીડિયા, 2008
- વેરેન્ટસેવા એલ.જી. અકાર્બનિક, ભૌતિક અને કોલોઇડલ રસાયણશાસ્ત્ર, (ચકાસણી પરીક્ષણો) 2009
વધારાનું સાહિત્ય:
- રવિચ-શેરબો એમ.આઈ., નોવિકોવ વી.વી. ભૌતિક અને કોલોઇડલ રસાયણશાસ્ત્ર. એમ. 2003.
2. સ્લેસારેવ વી.આઈ. રસાયણશાસ્ત્ર. જીવંત રસાયણશાસ્ત્રની મૂળભૂત બાબતો. સેન્ટ પીટર્સબર્ગ: ખમીઝદાત, 2001
3. એર્શોવ યુ.એ. સામાન્ય રસાયણશાસ્ત્ર. બાયોફિઝિકલ કેમિસ્ટ્રી. બાયોજેનિક તત્વોની રસાયણશાસ્ત્ર. એમ.: વીએસએચ, 2003.
4. આસનબેવા આર.ડી., ઇલ્યાસોવા એમ.આઈ. જૈવિક રીતે મહત્વપૂર્ણ કાર્બનિક સંયોજનોની રચના અને પ્રતિક્રિયાશીલતાના સૈદ્ધાંતિક પાયા. અલ્માટી, 2003.
- બાયોઓર્ગેનિક રસાયણશાસ્ત્રમાં પ્રયોગશાળા વર્ગોની માર્ગદર્શિકા, ઇડી. પર. ટ્યુકાવકીના. એમ., બસ્ટાર્ડ, 2003.
- ગ્લિન્કા એન.એલ. સામાન્ય રસાયણશાસ્ત્ર. એમ., 2003.
- પોનોમારેવ વી.ડી. વિશ્લેષણાત્મક રસાયણશાસ્ત્ર ભાગ 1, 2 2003
6. પરીક્ષણ પ્રશ્નો (પ્રતિસાદ):
1. સમગ્ર રીતે પોલિપેપ્ટાઇડ સાંકળની રચના શું નક્કી કરે છે?
2. પ્રોટીન ડિનેચરેશન શું તરફ દોરી જાય છે?
3. આઇસોઇલેક્ટ્રિક પોઇન્ટ શું કહેવાય છે?
4. કયા એમિનો એસિડને આવશ્યક કહેવામાં આવે છે?
5. આપણા શરીરમાં પ્રોટીન કેવી રીતે બને છે?
સંબંધિત માહિતી.
એમિનો એસિડ એ કાર્બનિક એમ્ફોટેરિક સંયોજનો છે. તેઓ પરમાણુમાં વિપરીત પ્રકૃતિના બે કાર્યાત્મક જૂથો ધરાવે છે: મૂળભૂત ગુણધર્મો સાથે એમિનો જૂથ અને એસિડિક ગુણધર્મો સાથે કાર્બોક્સિલ જૂથ. એમિનો એસિડ એસિડ અને બેઝ બંને સાથે પ્રતિક્રિયા આપે છે:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
જ્યારે એમિનો એસિડ પાણીમાં ઓગળી જાય છે, ત્યારે કાર્બોક્સિલ જૂથ હાઇડ્રોજન આયનને દૂર કરે છે, જે એમિનો જૂથ સાથે જોડી શકે છે. આ કિસ્સામાં, આંતરિક મીઠું રચાય છે, જેનું પરમાણુ દ્વિધ્રુવી આયન છે:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO - .
વિવિધ વાતાવરણમાં એમિનો એસિડના એસિડ-બેઝ રૂપાંતરણને નીચેના સામાન્ય ચિત્ર દ્વારા રજૂ કરી શકાય છે:

એમિનો એસિડના જલીય દ્રાવણમાં કાર્યકારી જૂથોની સંખ્યાના આધારે તટસ્થ, આલ્કલાઇન અથવા એસિડિક વાતાવરણ હોય છે. આમ, ગ્લુટામિક એસિડ એસિડિક દ્રાવણ બનાવે છે (બે -COOH જૂથો, એક -NH 2), લાયસિન એક આલ્કલાઇન દ્રાવણ બનાવે છે (એક -COOH જૂથ, બે -NH 2).
પ્રાથમિક એમાઇન્સની જેમ, એમિનો એસિડ નાઈટ્રસ એસિડ સાથે પ્રતિક્રિયા આપે છે, એમિનો જૂથ હાઇડ્રોક્સો જૂથમાં અને એમિનો એસિડ હાઇડ્રોક્સી એસિડમાં રૂપાંતરિત થાય છે:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
પ્રકાશિત નાઇટ્રોજનના જથ્થાને માપવાથી આપણે એમિનો એસિડની માત્રા નક્કી કરી શકીએ છીએ ( વેન Slyke પદ્ધતિ).
એમિનો એસિડ હાઇડ્રોજન ક્લોરાઇડ ગેસની હાજરીમાં આલ્કોહોલ સાથે પ્રતિક્રિયા કરી શકે છે, એસ્ટરમાં ફેરવાય છે (વધુ સ્પષ્ટ રીતે, એસ્ટરનું હાઇડ્રોક્લોરાઇડ મીઠું):
H 2 N-CH(R)-COOH + R'OH H 2 N-CH(R)-COOR' + H 2 O.
એમિનો એસિડ એસ્ટર્સ પાસે બાયપોલર માળખું નથી અને તે અસ્થિર સંયોજનો છે.
એમિનો એસિડની સૌથી મહત્વપૂર્ણ મિલકત પેપ્ટાઇડ્સ બનાવવા માટે ઘનીકરણ કરવાની તેમની ક્ષમતા છે.
ગુણાત્મક પ્રતિક્રિયાઓ.
1) બધા એમિનો એસિડ નિનહાઈડ્રિન દ્વારા ઓક્સિડાઇઝ થાય છે

વાદળી-વાયોલેટ રંગના ઉત્પાદનોની રચના સાથે. ઇમિનો એસિડ પ્રોલાઇન નિનહાઇડ્રિન સાથે પીળો રંગ આપે છે. આ પ્રતિક્રિયાનો ઉપયોગ સ્પેક્ટ્રોફોટોમેટ્રી દ્વારા એમિનો એસિડની માત્રા નક્કી કરવા માટે થઈ શકે છે.
2) જ્યારે સુગંધિત એમિનો એસિડને કેન્દ્રિત નાઈટ્રિક એસિડ સાથે ગરમ કરવામાં આવે છે, ત્યારે બેન્ઝીન રિંગનું નાઈટ્રેશન થાય છે અને પીળા રંગના સંયોજનો રચાય છે. આ પ્રતિક્રિયા કહેવામાં આવે છે ઝેન્થોપ્રોટીન(ગ્રીક ઝેન્થોસમાંથી - પીળો).
ગ્લાયસીન સિવાયના તમામ α-એમિનો એસિડમાં ચિરલ α-કાર્બન અણુ હોય છે અને તે આ રીતે થઈ શકે છે ઉત્તેજક:
એવું દર્શાવવામાં આવ્યું છે કે લગભગ તમામ કુદરતી એમિનો એસિડ્સ -કાર્બન અણુ પર સમાન સંબંધિત ગોઠવણી ધરાવે છે. -(-)-સેરીનનો કાર્બન અણુ પરંપરાગત રીતે સોંપવામાં આવ્યો હતો એલ-રૂપરેખાંકન, અને (+)-સેરીનનું -કાર્બન અણુ - ડી- રૂપરેખાંકન. તદુપરાંત, જો એમિનો એસિડનું ફિશર પ્રક્ષેપણ એવું લખવામાં આવે કે કાર્બોક્સિલ જૂથ ટોચ પર અને R તળિયે સ્થિત છે, તો પછી એલ-એમિનો એસિડ, એમિનો જૂથ ડાબી બાજુએ હશે, અને ડી- એમિનો એસિડ - જમણી બાજુએ. એમિનો એસિડ રૂપરેખાંકન નક્કી કરવા માટે ફિશરની યોજના એ તમામ α-એમિનો એસિડને લાગુ પડે છે જેમાં ચિરલ α-કાર્બન અણુ હોય છે.
આકૃતિ પરથી સ્પષ્ટ થાય છે કે એલ-એમિનો એસિડ રેડિકલની પ્રકૃતિને આધારે ડેક્સ્ટ્રોરોટેટરી (+) અથવા લેવોરોટેટરી (-) હોઈ શકે છે. કુદરતમાં મોટા ભાગના એમિનો એસિડ જોવા મળે છે એલ-પંક્તિ. તેમના enantiomorphs, એટલે કે ડીએમિનો એસિડ માત્ર સુક્ષ્મસજીવો દ્વારા સંશ્લેષણ કરવામાં આવે છે અને કહેવામાં આવે છે "અકુદરતી" એમિનો એસિડ.
(R,S) નામકરણ મુજબ, મોટાભાગના "કુદરતી" અથવા L-એમિનો એસિડમાં S રૂપરેખાંકન હોય છે.
L-Isoleucine અને L-threonine, પ્રત્યેક પરમાણુ દીઠ બે ચિરલ કેન્દ્રો ધરાવે છે, -કાર્બન અણુ પરના રૂપરેખાંકનના આધારે ડાયસ્ટેરિયોમર્સની જોડીના કોઈપણ સભ્ય હોઈ શકે છે. આ એમિનો એસિડની સાચી નિરપેક્ષ રૂપરેખાંકનો નીચે આપેલ છે.
એમિનો એસિડના એસિડ-બેઝ ગુણધર્મો
એમિનો એસિડ એ એમ્ફોટેરિક પદાર્થો છે જે કેશન અથવા આયનોના સ્વરૂપમાં અસ્તિત્વમાં હોઈ શકે છે. આ ગુણધર્મ બંને એસિડિકની હાજરી દ્વારા સમજાવવામાં આવે છે ( -COUNT), અને મુખ્ય ( -એનએચ 2 ) સમાન પરમાણુમાં જૂથો. ખૂબ જ એસિડિક ઉકેલોમાં એન.એચ. 2 એસિડ જૂથ પ્રોટોનેટેડ છે અને એસિડ કેશન બને છે. મજબૂત આલ્કલાઇન દ્રાવણમાં, એમિનો એસિડનું કાર્બોક્સિલ જૂથ ડિપ્રોટોનેટ થાય છે અને એસિડ એનિઓનમાં રૂપાંતરિત થાય છે.
નક્કર સ્થિતિમાં, એમિનો એસિડ સ્વરૂપમાં અસ્તિત્વ ધરાવે છે zwitterions (દ્વિધ્રુવી આયનો, આંતરિક ક્ષાર). ઝ્વિટરિયન્સમાં, પ્રોટોન કાર્બોક્સિલ જૂથમાંથી એમિનો જૂથમાં સ્થાનાંતરિત થાય છે:
જો તમે વાહક માધ્યમમાં એમિનો એસિડ મૂકો છો અને ત્યાં ઇલેક્ટ્રોડ્સની જોડી ઓછી કરો છો, તો પછી એસિડિક દ્રાવણમાં એમિનો એસિડ કેથોડમાં સ્થાનાંતરિત થશે, અને આલ્કલાઇન દ્રાવણમાં - એનોડમાં. આપેલ એમિનો એસિડના ચોક્કસ pH મૂલ્યની લાક્ષણિકતા પર, તે એનોડ અથવા કેથોડ તરફ આગળ વધશે નહીં, કારણ કે દરેક પરમાણુ ઝ્વિટરિયનના સ્વરૂપમાં છે (ધન અને નકારાત્મક બંને ચાર્જ વહન કરે છે). આ pH મૂલ્ય કહેવાય છે આઇસોઇલેક્ટ્રિક બિંદુઆપેલ એમિનો એસિડનું (pI).
એમિનો એસિડની પ્રતિક્રિયાઓ
એમિનો એસિડ લેબોરેટરીમાં પસાર થતી મોટાભાગની પ્રતિક્રિયાઓ ( ઇન વિટ્રો), તમામ એમાઇન્સ અથવા કાર્બોક્સિલિક એસિડની લાક્ષણિકતા.
1. કાર્બોક્સિલ જૂથમાં એમાઈડ્સની રચના. જ્યારે એમિનો એસિડનું કાર્બોનિલ જૂથ એમાઇનોના એમિનો જૂથ સાથે પ્રતિક્રિયા કરે છે, ત્યારે એમિનો એસિડની પોલિકન્ડેન્સેશન પ્રતિક્રિયા સમાંતર રીતે થાય છે, જે એમાઇડ્સની રચના તરફ દોરી જાય છે. પોલિમરાઇઝેશનને રોકવા માટે, એસિડના એમિનો જૂથને અવરોધિત કરવામાં આવે છે જેથી માત્ર એમાઇનો જૂથ જ પ્રતિક્રિયા કરે. આ હેતુ માટે, કાર્બોબેન્ઝોક્સીક્લોરાઇડ (કાર્બોબેન્ઝાઇલોક્સીક્લોરાઇડ, બેન્ઝિલ ક્લોરોફોર્મેટ) નો ઉપયોગ થાય છે. ઘસવું-બ્યુટોક્સીકાર્બોક્સાઝીડ, વગેરે. એમાઈન સાથે પ્રતિક્રિયા કરવા માટે, કાર્બોક્સિલ જૂથને એથિલ ક્લોરોફોર્મેટ સાથે સારવાર દ્વારા સક્રિય કરવામાં આવે છે. રક્ષણ જૂથપછી ઉત્પ્રેરક હાઇડ્રોજેનોલિસિસ દ્વારા અથવા એસિટિક એસિડમાં હાઇડ્રોજન બ્રોમાઇડના ઠંડા દ્રાવણની ક્રિયા દ્વારા દૂર કરવામાં આવે છે.

2. એમિનો જૂથમાં એમાઈડ્સની રચના. જ્યારે એમિનો એસિડનું એમિનો જૂથ એસીલેટેડ હોય છે, ત્યારે એમાઈડ બને છે.

મૂળભૂત માધ્યમમાં પ્રતિક્રિયા વધુ સારી રીતે આગળ વધે છે, કારણ કે આ મુક્ત એમાઈનની ઉચ્ચ સાંદ્રતાને સુનિશ્ચિત કરે છે.
3. એસ્ટરની રચના. એમિનો એસિડના કાર્બોક્સિલ જૂથને પરંપરાગત પદ્ધતિઓ દ્વારા સરળતાથી એસ્ટરિફાઇડ કરવામાં આવે છે. ઉદાહરણ તરીકે, મિથાઈલ એસ્ટર્સ ડ્રાય હાઈડ્રોજન ક્લોરાઈડ ગેસને મિથેનોલમાં એમિનો એસિડના દ્રાવણ દ્વારા પસાર કરીને તૈયાર કરવામાં આવે છે:

એમિનો એસિડ પોલીકોન્ડેન્સેશન માટે સક્ષમ છે, પરિણામે પોલિમાઇડની રચના થાય છે. એમિનો એસિડ ધરાવતા પોલિમાઇડ્સ કહેવામાં આવે છે પેપ્ટાઈડ્સ અથવા પોલિપેપ્ટાઇડ્સ . આવા પોલિમરમાં એમાઈડ બોન્ડ કહેવાય છે પેપ્ટાઇડ સંચાર. ઓછામાં ઓછા 5000 ના પરમાણુ વજનવાળા પોલિપેપ્ટાઇડ્સ કહેવામાં આવે છે પ્રોટીન . પ્રોટીનમાં લગભગ 25 અલગ અલગ એમિનો એસિડ હોય છે. જ્યારે આપેલ પ્રોટીનને હાઇડ્રોલાઇઝ કરવામાં આવે છે, ત્યારે આ તમામ એમિનો એસિડ અથવા તેમાંના કેટલાક વ્યક્તિગત પ્રોટીનની લાક્ષણિકતાના ચોક્કસ પ્રમાણમાં રચાય છે.
આપેલ પ્રોટીનમાં સહજ સાંકળમાં એમિનો એસિડ અવશેષોના અનન્ય ક્રમને કહેવામાં આવે છે પ્રાથમિક પ્રોટીન માળખું . પ્રોટીન પરમાણુઓની વળી જતી સાંકળોના લક્ષણો (અવકાશમાં ટુકડાઓની પરસ્પર ગોઠવણી) કહેવામાં આવે છે. પ્રોટીનની ગૌણ રચના . એમિનો એસિડ બાજુની સાંકળોને કારણે પ્રોટીનની પોલીપેપ્ટાઈડ સાંકળો એમાઈડ, ડાઈસલ્ફાઈડ, હાઈડ્રોજન અને અન્ય બોન્ડ બનાવવા માટે એકબીજા સાથે જોડાઈ શકે છે. પરિણામે, સર્પાકાર બોલમાં ટ્વિસ્ટ થાય છે. આ માળખાકીય લક્ષણ કહેવામાં આવે છે પ્રોટીન તૃતીય માળખું . જૈવિક પ્રવૃત્તિ પ્રદર્શિત કરવા માટે, કેટલાક પ્રોટીન્સે પહેલા મેક્રોકોમ્પ્લેક્સ બનાવવું જોઈએ ( ઓલિગોપ્રોટીન), જેમાં કેટલાક સંપૂર્ણ પ્રોટીન સબ્યુનિટ્સનો સમાવેશ થાય છે. ચતુર્થાંશ માળખું જૈવિક રીતે સક્રિય સામગ્રીમાં આવા મોનોમર્સના જોડાણની ડિગ્રી નક્કી કરે છે.
પ્રોટીનને બે મોટા જૂથોમાં વહેંચવામાં આવે છે - ફાઇબરિલર (પરમાણુની લંબાઈ અને પહોળાઈનો ગુણોત્તર 10 કરતા વધારે છે) અને ગોળાકાર (10 કરતા ઓછો ગુણોત્તર). ફાઈબ્રિલર પ્રોટીનનો સમાવેશ થાય છે કોલેજન , કરોડઅસ્થિધારી પ્રાણીઓમાં સૌથી વિપુલ પ્રમાણમાં પ્રોટીન; તે કોમલાસ્થિના શુષ્ક વજનના લગભગ 50% અને હાડકાના ઘન પદાર્થના લગભગ 30% જેટલો હિસ્સો ધરાવે છે. છોડ અને પ્રાણીઓની મોટાભાગની નિયમનકારી પ્રણાલીઓમાં, ઉત્પ્રેરક ગ્લોબ્યુલર પ્રોટીન દ્વારા કરવામાં આવે છે, જેને કહેવામાં આવે છે ઉત્સેચકો .
એમિનો એસિડના એસિડ-બેઝ ગુણધર્મો તેમની રચનામાં બે ionizable જૂથો - કાર્બોક્સિલ અને એમિનો જૂથોની હાજરી સાથે સંકળાયેલા છે, તેથી, એમિનો એસિડ એસિડ અને પાયા બંનેના ગુણધર્મો પ્રદર્શિત કરી શકે છે, એટલે કે. તેઓ એમ્ફોટેરિક સંયોજનો છે. સ્ફટિકીય સ્થિતિમાં અને જલીય દ્રાવણમાં, α-એમિનો એસિડ દ્વિધ્રુવી આયનોના સ્વરૂપમાં અસ્તિત્વ ધરાવે છે, જેને ઝ્વિટરિયન પણ કહેવાય છે. આયનીય માળખું α-એમિનો એસિડના કેટલાક ગુણધર્મો નક્કી કરે છે: ઉચ્ચ ગલનબિંદુ (200-300°C), બિન-અસ્થિરતા, પાણીમાં દ્રાવ્યતા અને બિન-ધ્રુવીય કાર્બનિક દ્રાવકોમાં અદ્રાવ્યતા. પાણીમાં એમિનો એસિડની દ્રાવ્યતા શરીરમાં તેમના શોષણ અને પરિવહન સાથે સંબંધિત છે. એમિનો એસિડ પરમાણુઓનું આયનીકરણ દ્રાવણના pH પર આધાર રાખે છે. મોનોએમિનોમોનોકાર્બોક્સિલિક એસિડ માટે, વિયોજન પ્રક્રિયા નીચેના સ્વરૂપ ધરાવે છે:
મજબૂત એસિડિક દ્રાવણમાં, એમિનો એસિડ હકારાત્મક આયન તરીકે હાજર હોય છે, અને આલ્કલાઇન દ્રાવણમાં તે નકારાત્મક આયન તરીકે હાજર હોય છે.
એમિનો એસિડના એસિડ-બેઝ ગુણધર્મોને એસિડ અને પાયાના બ્રૉન્સ્ટેડ-લોરી સિદ્ધાંતના આધારે સમજાવી શકાય છે. સંપૂર્ણ પ્રોટોનેટેડ -એમિનો એસિડ (કેશનિક સ્વરૂપ), બ્રૉન્સ્ટેડ થિયરીના પરિપ્રેક્ષ્યમાં, એક ડાયબેસિક એસિડ છે જેમાં બે એસિડ જૂથો છે: એક અસંબંધિત કાર્બોક્સિલ જૂથ (- COOH) અને પ્રોટોનેટેડ એમિનો જૂથ (NH 3), જે લાક્ષણિકતા ધરાવે છે. pK 1 અને pK 2 ના અનુરૂપ મૂલ્યો દ્વારા.
એમિનો એસિડ માટે pK મૂલ્યો ટાઇટ્રેશન વણાંકોથી નક્કી કરવામાં આવે છે. એલનાઇન ટાઇટ્રેશન વળાંક (ફિગ. 1) ને ધ્યાનમાં લો.

ચોખા. 1 – 0.1 M HCl સોલ્યુશન (a) અને 0.1 M NaOH સોલ્યુશન (b) સાથે 0.1 M એલનાઇન સોલ્યુશનને ટાઇટ્રેટ કરીને મેળવેલ વળાંક.
એલેનાઇનના ટાઇટ્રેશન કર્વ પરથી તે અનુસરે છે કે કાર્બોક્સિલ જૂથમાં pK 1 = 2.34 છે, અને પ્રોટોનેટેડ એમિનો જૂથમાં pK 2 = 9.69 છે. pH = 6.02 પર, જ્યારે કણનો કુલ વિદ્યુત ચાર્જ 0 હોય ત્યારે એલનાઇન દ્વિધ્રુવી આયન તરીકે અસ્તિત્વ ધરાવે છે. આ pH મૂલ્ય પર, એલાનિન પરમાણુ ઇલેક્ટ્રિકલી ન્યુટ્રલ હોય છે. આ pH મૂલ્યને આઇસોઇલેક્ટ્રિક બિંદુ કહેવામાં આવે છે અને તેને pH et અથવા piI તરીકે સૂચિત કરવામાં આવે છે. મોનોએમિનોમોનોકાર્બોક્સિલિક એસિડ્સ માટે, આઇસોઇલેક્ટ્રિક બિંદુની ગણતરી બે pK મૂલ્યોના અંકગણિત સરેરાશ તરીકે કરવામાં આવે છે. ઉદાહરણ તરીકે, એલનાઇન માટે તે બરાબર છે:
рI= ½(рК 1 + рК 2) = ½(2.34 + 9.69) = 6.02
આઇસોઇલેક્ટ્રિક બિંદુથી ઉપરના pH મૂલ્ય પર, એમિનો એસિડ નકારાત્મક રીતે ચાર્જ થાય છે, અને pI ની નીચે pH મૂલ્ય પર, એમિનો એસિડ ચોખ્ખો હકારાત્મક ચાર્જ વહન કરે છે. ઉદાહરણ તરીકે, pH = 1.0 પર, બધા એલાનિન પરમાણુઓ આયનોના સ્વરૂપમાં અસ્તિત્વ ધરાવે છે

+1 ના કુલ ચાર્જ સાથે. pH = 2.34 પર, જ્યારે સમાન પ્રમાણમાં આયનોનું મિશ્રણ હોય છે

કુલ ચાર્જ = +0.5. એ જ રીતે, તમે કોઈપણ pH મૂલ્ય પર કોઈપણ અન્ય એમિનો એસિડ માટે કુલ ચાર્જની નિશાની અને તીવ્રતાની આગાહી કરી શકો છો.
રેડિકલમાં આયનોઇઝેબલ જૂથ સાથેના એમિનો એસિડમાં વધુ જટિલ ટાઇટ્રેશન વણાંકો હોય છે, જેમાં આયનીકરણના ત્રણ સંભવિત તબક્કાઓને અનુરૂપ 3 વિભાગો હોય છે, અને તેથી, તેમની પાસે ત્રણ pK મૂલ્યો હોય છે (pK 1, pK 2 અને pK આર). એસિડિક એમિનો એસિડનું આયનીકરણ, જેમ કે એસ્પાર્ટિક એસિડ, નીચેના ક્રમિક તબક્કાઓનો સમાવેશ કરે છે:

આવા એમિનો એસિડના આઇસોઇલેક્ટ્રિક બિંદુઓ -એમિનો અને -કાર્બોક્સિલ જૂથો સાથે રેડિકલના ionizable જૂથની હાજરી દ્વારા પણ નક્કી કરવામાં આવે છે. મોનોએમિનોડિકાર્બોક્સિલિક એસિડ્સ માટે, આઇસોઇલેક્ટ્રિક બિંદુઓ એસિડિક pH પ્રદેશમાં સ્થાનાંતરિત થાય છે અને બે કાર્બોક્સિલ જૂથો (pIaspartic acid = 2.97) માટે pK મૂલ્યો વચ્ચેના અંકગણિત સરેરાશ તરીકે વ્યાખ્યાયિત કરવામાં આવે છે. મૂળભૂત એમિનો એસિડ માટે, પીઆઈને આલ્કલાઇન પ્રદેશમાં સ્થાનાંતરિત કરવામાં આવે છે અને બે પ્રોટોનેટેડ એમિનો જૂથો (પીઆઈલીસીન = 9.74) માટે પીકે મૂલ્યો વચ્ચેના અંકગણિત સરેરાશ તરીકે ગણવામાં આવે છે.
એમિનો એસિડના એસિડ-બેઝ ગુણધર્મોનો ઉપયોગ ઇલેક્ટ્રોફોરેસીસ અને આયન વિનિમય ક્રોમેટોગ્રાફી દ્વારા એમિનો એસિડને અલગ કરવા અને અનુગામી ઓળખ માટે થાય છે. આ બંને પદ્ધતિઓ આપેલ pH મૂલ્ય પર કુલ વિદ્યુત ચાર્જના સંકેત અને તીવ્રતામાં તફાવત પર આધારિત છે.