એમિનો એસિડ એ કાર્બનિક એમ્ફોટેરિક સંયોજનો છે. તેઓ પરમાણુમાં વિપરીત પ્રકૃતિના બે કાર્યાત્મક જૂથો ધરાવે છે: મૂળભૂત ગુણધર્મો સાથે એમિનો જૂથ અને એસિડિક ગુણધર્મો સાથે કાર્બોક્સિલ જૂથ. એમિનો એસિડ એસિડ અને બેઝ બંને સાથે પ્રતિક્રિયા આપે છે:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
જ્યારે એમિનો એસિડ પાણીમાં ઓગળી જાય છે, ત્યારે કાર્બોક્સિલ જૂથ હાઇડ્રોજન આયનને દૂર કરે છે, જે એમિનો જૂથ સાથે જોડી શકે છે. આ કિસ્સામાં, આંતરિક મીઠું રચાય છે, જેનું પરમાણુ દ્વિધ્રુવી આયન છે:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO – .
વિવિધ વાતાવરણમાં એમિનો એસિડના એસિડ-બેઝ રૂપાંતરણને નીચેના સામાન્ય ચિત્ર દ્વારા રજૂ કરી શકાય છે:
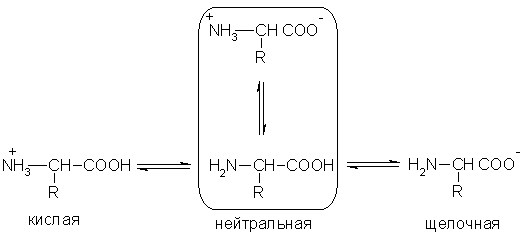
એમિનો એસિડના જલીય દ્રાવણમાં કાર્યાત્મક જૂથોની સંખ્યાના આધારે તટસ્થ, આલ્કલાઇન અથવા એસિડિક વાતાવરણ હોય છે. આમ, ગ્લુટામિક એસિડ એસિડિક દ્રાવણ બનાવે છે (બે -COOH જૂથો, એક -NH 2), લાયસિન એક આલ્કલાઇન દ્રાવણ બનાવે છે (એક -COOH જૂથ, બે -NH 2).
પ્રાથમિક એમાઇન્સની જેમ, એમિનો એસિડ નાઈટ્રસ એસિડ સાથે પ્રતિક્રિયા આપે છે, એમિનો જૂથ હાઇડ્રોક્સો જૂથમાં અને એમિનો એસિડ હાઇડ્રોક્સી એસિડમાં રૂપાંતરિત થાય છે:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
પ્રકાશિત નાઇટ્રોજનના જથ્થાને માપવાથી આપણે એમિનો એસિડનું પ્રમાણ નક્કી કરી શકીએ છીએ ( વેન Slyke પદ્ધતિ).
એમિનો એસિડ હાઇડ્રોજન ક્લોરાઇડ ગેસની હાજરીમાં આલ્કોહોલ સાથે પ્રતિક્રિયા કરી શકે છે, એસ્ટરમાં ફેરવાય છે (વધુ સ્પષ્ટ રીતે, એસ્ટરનું હાઇડ્રોક્લોરાઇડ મીઠું):
H 2 N-CH(R)-COOH + R'OH H 2 N-CH(R)-COOR' + H 2 O.
એમિનો એસિડ એસ્ટર્સ પાસે બાયપોલર માળખું નથી અને તે અસ્થિર સંયોજનો છે.
એમિનો એસિડની સૌથી મહત્વપૂર્ણ મિલકત પેપ્ટાઇડ્સ બનાવવા માટે ઘનીકરણ કરવાની તેમની ક્ષમતા છે.
ગુણાત્મક પ્રતિક્રિયાઓ.
1) બધા એમિનો એસિડ નિનહાઇડ્રેન દ્વારા ઓક્સિડાઇઝ થાય છે

વાદળી-વાયોલેટ રંગના ઉત્પાદનોની રચના સાથે. ઇમિનો એસિડ પ્રોલાઇન નિનહાઇડ્રિન સાથે પીળો રંગ આપે છે. આ પ્રતિક્રિયાનો ઉપયોગ સ્પેક્ટ્રોફોટોમેટ્રી દ્વારા એમિનો એસિડની માત્રા નક્કી કરવા માટે થઈ શકે છે.
2) જ્યારે સુગંધિત એમિનો એસિડને કેન્દ્રિત નાઈટ્રિક એસિડ સાથે ગરમ કરવામાં આવે છે, ત્યારે બેન્ઝીન રિંગનું નાઈટ્રેશન થાય છે અને પીળા રંગના સંયોજનો રચાય છે. આ પ્રતિક્રિયા કહેવામાં આવે છે ઝેન્થોપ્રોટીન(ગ્રીક ઝેન્થોસમાંથી - પીળો).
બધા કુદરતી એમિનો એસિડને નીચેના મુખ્ય જૂથોમાં વિભાજિત કરી શકાય છે:
1) એલિફેટિક સંતૃપ્ત એમિનો એસિડ(ગ્લાયસીન, એલનાઇન);
2) સલ્ફર ધરાવતા એમિનો એસિડ(સિસ્ટીન);
3) એલિફેટિક હાઇડ્રોક્સિલ જૂથ સાથે એમિનો એસિડ(સેરીન);
4) સુગંધિત એમિનો એસિડ(ફેનીલાલેનાઇન, ટાયરોસિન);
5) એસિડ રેડિકલ સાથે એમિનો એસિડ(ગ્લુટામિક એસિડ);
6) મૂળભૂત રેડિકલ સાથે એમિનો એસિડ(લાયસિન).
આઇસોમેરિઝમ.તમામ એ-એમિનો એસિડમાં, ગ્લાયસીન સિવાય, એ-કાર્બન અણુ ચાર અલગ-અલગ અવેજીઓ સાથે જોડાયેલ છે, તેથી આ તમામ એમિનો એસિડ બે આઇસોમરના સ્વરૂપમાં અસ્તિત્વમાં હોઈ શકે છે, જે એકબીજાની પ્રતિબિંબ છે.
રસીદ. 1. પ્રોટીનનું હાઇડ્રોલિસિસસામાન્ય રીતે એમિનો એસિડનું જટિલ મિશ્રણ ઉત્પન્ન કરે છે. જો કે, અસંખ્ય પદ્ધતિઓ વિકસાવવામાં આવી છે જે જટિલ મિશ્રણમાંથી વ્યક્તિગત શુદ્ધ એમિનો એસિડ મેળવવાનું શક્ય બનાવે છે.
2. એમિનો જૂથ સાથે હેલોજનની બદલીઅનુરૂપ હેલોજન એસિડમાં. એમિનો એસિડ મેળવવાની આ પદ્ધતિ એલ્કેન્સ અને એમોનિયાના હેલોજન ડેરિવેટિવ્ઝમાંથી એમાઇન્સ મેળવવા માટે સંપૂર્ણપણે સમાન છે:
ભૌતિક ગુણધર્મો.એમિનો એસિડ ઘન સ્ફટિકીય પદાર્થો છે, જે પાણીમાં અત્યંત દ્રાવ્ય અને કાર્બનિક દ્રાવકોમાં સહેજ દ્રાવ્ય છે. ઘણા એમિનો એસિડનો સ્વાદ મીઠો હોય છે. તેઓ ઓગળે છે ઉચ્ચ તાપમાનઅને સામાન્ય રીતે પ્રક્રિયામાં વિઘટન થાય છે. તેઓ વરાળની સ્થિતિમાં જઈ શકતા નથી.
રાસાયણિક ગુણધર્મો. એમિનો એસિડ એ કાર્બનિક એમ્ફોટેરિક સંયોજનો છે.તેઓ પરમાણુમાં વિરોધી પ્રકૃતિના બે કાર્યાત્મક જૂથો ધરાવે છે: મૂળભૂત ગુણધર્મો સાથે એમિનો જૂથ અને એસિડિક ગુણધર્મો સાથે કાર્બોક્સિલ જૂથ. એમિનો એસિડ એસિડ અને બેઝ બંને સાથે પ્રતિક્રિયા આપે છે:
જ્યારે એમિનો એસિડ પાણીમાં ઓગળી જાય છે, ત્યારે કાર્બોક્સિલ જૂથ હાઇડ્રોજન આયનને દૂર કરે છે, જે એમિનો જૂથ સાથે જોડી શકે છે. આ બનાવે છે આંતરિક મીઠું,જેનું પરમાણુ દ્વિધ્રુવી આયન છે:
વિવિધ વાતાવરણમાં એમિનો એસિડના એસિડ-બેઝ રૂપાંતરણને નીચેના ચિત્ર દ્વારા રજૂ કરી શકાય છે:
એમિનો એસિડના જલીય દ્રાવણમાં કાર્યાત્મક જૂથોની સંખ્યાના આધારે તટસ્થ, આલ્કલાઇન અથવા એસિડિક વાતાવરણ હોય છે. આમ, ગ્લુટામિક એસિડ એસિડિક દ્રાવણ બનાવે છે (બે -COOH જૂથો, એક -NH 2), લાયસિન એક આલ્કલાઇન દ્રાવણ બનાવે છે (એક -COOH જૂથ, બે -NH 2).
એમિનો એસિડ હાઇડ્રોજન ક્લોરાઇડ ગેસની હાજરીમાં આલ્કોહોલ સાથે પ્રતિક્રિયા આપીને એસ્ટર બનાવે છે:
એમિનો એસિડની સૌથી મહત્વપૂર્ણ મિલકત પેપ્ટાઇડ્સ બનાવવા માટે ઘનીકરણ કરવાની તેમની ક્ષમતા છે.
પેપ્ટાઇડ્સ. પેપ્ટાઇડ્સ. બે અથવા વધુ એમિનો એસિડ પરમાણુઓના ઘનીકરણ ઉત્પાદનો છે. બે એમિનો એસિડ અણુઓ પાણીના અણુને દૂર કરવા માટે એકબીજા સાથે પ્રતિક્રિયા કરી શકે છે અને એક ઉત્પાદન બનાવે છે જેમાં ટુકડાઓ જોડાયેલા હોય છે. પેપ્ટાઇડ બોન્ડ-CO-NH-.
પરિણામી સંયોજનને ડિપેપ્ટાઇડ કહેવામાં આવે છે. ડિપેપ્ટાઇડ પરમાણુ, એમિનો એસિડની જેમ, એમિનો જૂથ અને કાર્બોક્સિલ જૂથ ધરાવે છે અને વધુ એક એમિનો એસિડ પરમાણુ સાથે પ્રતિક્રિયા કરી શકે છે:
પ્રતિક્રિયા ઉત્પાદનને ટ્રિપેપ્ટાઇડ કહેવામાં આવે છે. પેપ્ટાઇડ સાંકળને વધારવાની પ્રક્રિયા સૈદ્ધાંતિક રીતે અનિશ્ચિત રૂપે ચાલુ રહી શકે છે (પોલીકડેન્સેશન) અને ખૂબ ઊંચા પરમાણુ વજન (પ્રોટીન) વાળા પદાર્થો તરફ દોરી જાય છે.
પેપ્ટાઇડ્સની મુખ્ય મિલકત હાઇડ્રોલિઝ કરવાની ક્ષમતા છે.હાઇડ્રોલિસિસ દરમિયાન, પેપ્ટાઇડ સાંકળનો સંપૂર્ણ અથવા આંશિક ક્લીવેજ થાય છે અને ઓછા પરમાણુ વજનવાળા ટૂંકા પેપ્ટાઇડ્સ અથવા α-એમિનો એસિડ કે જે સાંકળ બનાવે છે તે રચાય છે. સંપૂર્ણ હાઇડ્રોલિસિસના ઉત્પાદનોનું વિશ્લેષણ અમને પેપ્ટાઇડની એમિનો એસિડ રચના નક્કી કરવા દે છે. જ્યારે પેપ્ટાઇડને કેન્દ્રિત હાઇડ્રોક્લોરિક એસિડ સાથે લાંબા સમય સુધી ગરમ કરવામાં આવે ત્યારે સંપૂર્ણ હાઇડ્રોલિસિસ થાય છે.
પેપ્ટાઇડ્સનું હાઇડ્રોલિસિસ એસિડિક અથવા આલ્કલાઇન વાતાવરણમાં તેમજ ઉત્સેચકોની ક્રિયા હેઠળ થઈ શકે છે. એમિનો એસિડ ક્ષાર એસિડિક અને આલ્કલાઇન વાતાવરણમાં રચાય છે:
એન્ઝાઇમેટિક હાઇડ્રોલિસિસ મહત્વપૂર્ણ છે કારણ કે તે થાય છે પસંદગીપૂર્વક,ટી . e. પેપ્ટાઇડ સાંકળના સખત રીતે વ્યાખ્યાયિત વિભાગોના ક્લીવેજને મંજૂરી આપે છે.
એમિનો એસિડ માટે ગુણાત્મક પ્રતિક્રિયાઓ. 1)બધા એમિનો એસિડ ઓક્સિડાઇઝ્ડ છે ninhydrinવાદળી-વાયોલેટ રંગના ઉત્પાદનોની રચના સાથે. આ પ્રતિક્રિયાનો ઉપયોગ સ્પેક્ટ્રોફોટોમેટ્રી દ્વારા એમિનો એસિડની માત્રા નક્કી કરવા માટે થઈ શકે છે. 2) જ્યારે સુગંધિત એમિનો એસિડને કેન્દ્રિત નાઈટ્રિક એસિડ સાથે ગરમ કરવામાં આવે છે, ત્યારે બેન્ઝીન રિંગનું નાઈટ્રેશન થાય છે અને પીળા રંગના સંયોજનો રચાય છે. આ પ્રતિક્રિયા કહેવામાં આવે છે ઝેન્થોપ્રોટીન(ગ્રીકમાંથી ઝેન્થોસ -પીળો).
ખિસકોલી. પ્રોટીન સાથે કુદરતી પોલિપેપ્ટાઇડ્સ છે ઉચ્ચ મૂલ્યોપરમાણુ વજન (10,000 થી લાખો સુધી). તેઓ તમામ જીવંત જીવોનો ભાગ છે અને વિવિધ જૈવિક કાર્યો કરે છે.
માળખું.પોલિપેપ્ટાઇડ સાંકળની રચનામાં ચાર સ્તરો ઓળખી શકાય છે. પ્રોટીનનું પ્રાથમિક માળખું પોલિપેપ્ટાઇડ સાંકળમાં એમિનો એસિડનો ચોક્કસ ક્રમ છે. પેપ્ટાઇડ સાંકળ માત્ર થોડી સંખ્યામાં પ્રોટીનમાં રેખીય માળખું ધરાવે છે. મોટાભાગના પ્રોટીનમાં, પેપ્ટાઇડ સાંકળ અવકાશમાં ચોક્કસ રીતે ફોલ્ડ કરવામાં આવે છે.
ગૌણ માળખું એ પોલિપેપ્ટાઇડ સાંકળનું સ્વરૂપ છે, એટલે કે NH અને CO જૂથો વચ્ચેના હાઇડ્રોજન બોન્ડને કારણે અવકાશમાં સાંકળ જે રીતે વળી જાય છે. સાંકળ નાખવાની મુખ્ય પદ્ધતિ સર્પાકાર છે.
પ્રોટીનનું તૃતીય માળખું એ અવકાશમાં ટ્વિસ્ટેડ હેલિક્સનું ત્રિ-પરિમાણીય રૂપરેખાંકન છે.પોલીપેપ્ટાઈડ સાંકળના વિવિધ સ્થળોએ સ્થિત સિસ્ટીન અવશેષો વચ્ચેના ડાયસલ્ફાઇડ પુલ -S-S-ને કારણે તૃતીય માળખું રચાય છે. તૃતીય માળખાના નિર્માણમાં પણ સામેલ છે આયનીય ક્રિયાપ્રતિક્રિયાઓવિરુદ્ધ ચાર્જ થયેલ જૂથો NH 3 + અને COO- અને હાઇડ્રોફોબિક ક્રિયાપ્રતિક્રિયાઓ, એટલે કે, પ્રોટીન પરમાણુને ફોલ્ડ કરવાની વૃત્તિ જેથી હાઇડ્રોફોબિક હાઇડ્રોકાર્બન અવશેષો બંધારણની અંદર હોય.
તૃતીય માળખું એ પ્રોટીનની અવકાશી સંસ્થાનું સર્વોચ્ચ સ્વરૂપ છે.જો કે, કેટલાક પ્રોટીન (ઉદાહરણ તરીકે, હિમોગ્લોબિન) હોય છે ચતુર્થાંશ માળખું, જે વિવિધ પોલિપેપ્ટાઇડ સાંકળો વચ્ચેની ક્રિયાપ્રતિક્રિયાને કારણે રચાય છે.
ભૌતિક ગુણધર્મોપ્રોટીન ખૂબ જ વૈવિધ્યસભર છે અને તેમની રચના દ્વારા નક્કી કરવામાં આવે છે. તેમના ભૌતિક ગુણધર્મોના આધારે, પ્રોટીનને બે વર્ગોમાં વહેંચવામાં આવે છે: ગ્લોબ્યુલર પ્રોટીનપાણીમાં ભળે છે અથવા કોલોઇડલ સોલ્યુશન બનાવે છે, ફાઇબરિલર પ્રોટીનપાણીમાં અદ્રાવ્ય.
રાસાયણિક ગુણધર્મો. 1 . પ્રાથમિક માળખું જાળવી રાખતી વખતે પ્રોટીનની ગૌણ અને તૃતીય રચનાના વિનાશને વિકૃતિકરણ કહેવામાં આવે છે. . જ્યારે ગરમ થાય છે, પર્યાવરણની એસિડિટીમાં ફેરફાર થાય છે અથવા રેડિયેશનના સંપર્કમાં આવે છે ત્યારે તે થાય છે. જ્યારે ઈંડા ઉકાળવામાં આવે છે ત્યારે ઈંડાની સફેદીનું કોગ્યુલેશન એ વિકૃતીકરણનું ઉદાહરણ છે. વિકૃતિકરણ ઉલટાવી શકાય તેવું અથવા ઉલટાવી શકાય તેવું હોઈ શકે છે.જ્યારે પ્રોટીન ભારે ધાતુઓના ક્ષાર - સીસા અથવા પારાના સંપર્કમાં આવે છે ત્યારે અદ્રાવ્ય પદાર્થોની રચનાને કારણે ઉલટાવી શકાય તેવું વિકૃતિકરણ થઈ શકે છે.
2. પ્રોટીન જલવિચ્છેદન એ એમિનો એસિડની રચના સાથે એસિડિક અથવા આલ્કલાઇન દ્રાવણમાં પ્રાથમિક બંધારણનો અફર વિનાશ છે. હાઇડ્રોલિસિસ ઉત્પાદનોનું વિશ્લેષણ કરીને, પ્રોટીનની માત્રાત્મક રચના નક્કી કરવી શક્ય છે.
3. પ્રોટીન માટે, ઘણા જાણીતા છે ગુણાત્મક પ્રતિક્રિયાઓ. પેપ્ટાઇડ બોન્ડ ધરાવતા તમામ સંયોજનો જ્યારે આલ્કલાઇન દ્રાવણમાં કોપર (II) ક્ષારના સંપર્કમાં આવે ત્યારે વાયોલેટ રંગ આપે છે. આ પ્રતિક્રિયા કહેવામાં આવે છે બ્યુરેટસુગંધિત એમિનો એસિડ અવશેષો (ફેનીલાલેનાઇન, ટાયરોસિન) ધરાવતા પ્રોટીન જ્યારે કેન્દ્રિત નાઈટ્રિક એસિડના સંપર્કમાં આવે ત્યારે પીળો રંગ આપે છે (ઝેન્થોપ્રોટીનપ્રતિક્રિયા).
પ્રોટીનનું જૈવિક મહત્વ:
1. સંપૂર્ણપણે શરીરમાં તમામ રાસાયણિક પ્રતિક્રિયાઓ ઉત્પ્રેરકની હાજરીમાં થાય છે - ઉત્સેચકોબધા જાણીતા ઉત્સેચકો છે પ્રોટીન પરમાણુઓ. પ્રોટીન ખૂબ શક્તિશાળી અને પસંદગીયુક્ત ઉત્પ્રેરક છે. તેઓ પ્રતિક્રિયાઓને લાખો વખત ઝડપી બનાવે છે, અને દરેક પ્રતિક્રિયાનું પોતાનું એક એન્ઝાઇમ હોય છે.
2. કેટલાક પ્રોટીન પરિવહન કાર્યો કરે છે અને પરમાણુઓ અથવા આયનોને સંશ્લેષણ અથવા સંચયના સ્થળો પર પરિવહન કરે છે. ઉદાહરણ તરીકે, લોહીમાં સમાયેલ પ્રોટીન હિમોગ્લોબિનપેશીઓ અને પ્રોટીનમાં ઓક્સિજન વહન કરે છે મ્યોગ્લોબિનસ્નાયુઓમાં ઓક્સિજનનો સંગ્રહ કરે છે.
3. પ્રોટીન છે બાંધકામ સામગ્રીકોષો તેમાંથી સહાયક, સ્નાયુઓ અને ઇન્ટિગ્યુમેન્ટરી પેશીઓ બનાવવામાં આવે છે.
4. માં પ્રોટીન મહત્વપૂર્ણ ભૂમિકા ભજવે છે રોગપ્રતિકારક તંત્રશરીર ચોક્કસ પ્રોટીન હોય છે (એન્ટિબોડીઝ),જે વિદેશી વસ્તુઓને ઓળખવા અને બાંધવામાં સક્ષમ છે - વાયરસ, બેક્ટેરિયા, વિદેશી કોષો.
5. રીસેપ્ટર પ્રોટીન પડોશી કોશિકાઓ અથવા તેમાંથી આવતા સંકેતોને સમજે છે અને પ્રસારિત કરે છે પર્યાવરણ. ઉદાહરણ તરીકે, આંખના રેટિના પર પ્રકાશની અસર ફોટોરિસેપ્ટર રોડોપ્સિન દ્વારા જોવામાં આવે છે. એસિટિલકોલાઇન જેવા ઓછા પરમાણુ વજનના પદાર્થો દ્વારા સક્રિય થયેલ રીસેપ્ટર્સ ચેતા કોષોના જંકશન પર ચેતા આવેગ પ્રસારિત કરે છે.
પ્રોટીનના કાર્યોની ઉપરોક્ત સૂચિમાંથી તે સ્પષ્ટ છે કે પ્રોટીન કોઈપણ જીવતંત્ર માટે મહત્વપૂર્ણ છે અને તેથી, તે સૌથી મહત્વપૂર્ણ છે. અભિન્ન ભાગખાદ્ય ઉત્પાદનો. પાચન પ્રક્રિયા દરમિયાન, પ્રોટીનને એમિનો એસિડમાં હાઇડ્રોલાઇઝ કરવામાં આવે છે, જે આપેલ જીવતંત્ર માટે જરૂરી પ્રોટીનના સંશ્લેષણ માટે પ્રારંભિક સામગ્રી તરીકે સેવા આપે છે. ત્યાં એમિનો એસિડ્સ છે જે શરીર પોતાને સંશ્લેષણ કરવામાં સક્ષમ નથી અને તેમને ફક્ત ખોરાક સાથે પ્રાપ્ત કરે છે.આ એમિનો એસિડ કહેવાય છે બદલી ન શકાય તેવું
વ્યાખ્યાન: સામાન્ય માહિતીપોલિમર અને તેમના વર્ગીકરણ વિશે.
એમિનો એસિડ એ સંયોજનો છે જે પરમાણુમાં એમિનો જૂથ અને કાર્બોક્સિલ જૂથ બંને ધરાવે છે. એમિનો એસિડનો સૌથી સરળ પ્રતિનિધિ એમિનોએસેટિક (ગ્લાયસીન) એસિડ છે: NH 2 -CH 2 -COOH
એમિનો એસિડમાં બે કાર્યાત્મક જૂથો હોવાથી, તેમના ગુણધર્મો અણુઓના આ જૂથો પર આધારિત છે: NH 2 - અને -COOH. એમિનો એસિડ એમ્ફોટેરિક છે કાર્બનિક પદાર્થ, આધાર તરીકે અને એસિડ તરીકે પ્રતિક્રિયા આપે છે.
ભૌતિક ગુણધર્મો.
એમિનો એસિડ એ રંગહીન સ્ફટિકીય પદાર્થો છે, જે પાણીમાં અત્યંત દ્રાવ્ય અને કાર્બનિક દ્રાવકોમાં સહેજ દ્રાવ્ય છે. ઘણા એમિનો એસિડનો સ્વાદ મીઠો હોય છે.
રાસાયણિક ગુણધર્મો
એસિડ (મૂળભૂત ગુણધર્મો દેખાય છે)
મેદાન
+મેટલ ઓક્સાઇડએમિનો એસિડ - પેપ્ટાઇડ્સની રચના
જો એમિનો જૂથો અને કાર્બોક્સિલ જૂથોની સંખ્યા સમાન હોય તો એમિનો એસિડ સૂચકનો રંગ બદલતા નથી.
1) NH 2 -CH 2 -COOH + HCl → NH 3 Cl-CH 2 -COOH
2) NH 2 -CH 2 -COOH + NaOH → NH 2 -CH 2 -COONa + H 2 O
3) NH 2 -CH 2 -COOH + NH 2 -CH 2 -COOH → NH 2 -CH 2 -CO NH-CH 2 -COOH + H 2 O
એમિનો એસિડની જૈવિક ભૂમિકા એ છે કે પ્રોટીનનું પ્રાથમિક માળખું તેમના અવશેષોમાંથી રચાય છે. ત્યાં 20 એમિનો એસિડ છે, જે આપણા શરીરમાં પ્રોટીનના ઉત્પાદન માટે પ્રારંભિક સામગ્રી છે. કેટલાક એમિનો એસિડનો ઉપયોગ ઉપચારાત્મક એજન્ટ તરીકે થાય છે, ઉદાહરણ તરીકે ગ્લુટામિક એસિડ - નર્વસ રોગો માટે, હિસ્ટિડિન - પેટના અલ્સર માટે. કેટલાક એમિનો એસિડનો ઉપયોગ ખાદ્ય ઉદ્યોગમાં થાય છે; તે તૈયાર ખોરાકમાં ઉમેરવામાં આવે છે અને ખોરાકમાં સુધારો કરવા માટે ખોરાક કેન્દ્રિત કરવામાં આવે છે.
ટિકિટ નંબર 16
એનિલિન એ એમાઇન્સનો પ્રતિનિધિ છે. રાસાયણિક માળખું અને ગુણધર્મો, તૈયારી અને વ્યવહારુ એપ્લિકેશન.
એમાઇન્સ છે કાર્બનિક સંયોજનો, જે એમોનિયાના ડેરિવેટિવ્ઝ છે, જેના પરમાણુમાં એક, બે અથવા ત્રણ હાઇડ્રોજન અણુઓ હાઇડ્રોકાર્બન રેડિકલ દ્વારા બદલવામાં આવે છે.
સામાન્ય સૂત્ર:
ભૌતિક ગુણધર્મો.
એનિલિન એ નબળા લાક્ષણિક ગંધ સાથે રંગહીન તેલયુક્ત પ્રવાહી છે, જે પાણીમાં સહેજ દ્રાવ્ય છે, પરંતુ આલ્કોહોલ, ઈથર અને બેન્ઝીનમાં દ્રાવ્ય છે. ઉત્કલન બિંદુ 184 ° સે. એનિલિન એ એક મજબૂત ઝેર છે જે લોહીને અસર કરે છે..
રાસાયણિક ગુણધર્મો.
એસિડ્સ (એમિનો જૂથ પર પ્રતિક્રિયાઓ)
Br 2 (જલીય દ્રાવણ)
C 6 H 5 NH 2 + HCl → C 6 H 5 NH 3 Cl
એનિલિનના રાસાયણિક ગુણધર્મો તેના એમિનો જૂથ -NH 2 અને બેન્ઝીન રિંગના પરમાણુમાં હાજરીને કારણે છે, જે પરસ્પર એકબીજાને પ્રભાવિત કરે છે.
રસીદ.
નાઇટ્રો સંયોજનોમાં ઘટાડો - ઝીનીન પ્રતિક્રિયા
C 6 H 5 NO 2 + H 2 → C 6 H 5 NH 2 + H 2 O
અરજી.
એનિલિનનો ઉપયોગ ફોટોગ્રાફિક સામગ્રી અને એનિલિન રંગોના ઉત્પાદનમાં થાય છે. પોલિમર, વિસ્ફોટકો અને દવાઓ મેળવવામાં આવે છે.
ટિકિટ નંબર 17
પ્રોટીન બાયોપોલિમર્સ જેવા છે. પ્રોટીનનું માળખું, ગુણધર્મો અને જૈવિક કાર્યો.
ખિસકોલી (પ્રોટીન, પોલિપેપ્ટાઇડ્સ) - પેપ્ટાઇડ બોન્ડ્સ દ્વારા સાંકળમાં જોડાયેલા એમિનો એસિડ ધરાવતા ઉચ્ચ-પરમાણુ કાર્બનિક પદાર્થો. જીવંત જીવોમાં, પ્રોટીનની એમિનો એસિડ રચના નક્કી કરવામાં આવે છે આનુવંશિક કોડ, મોટાભાગના કિસ્સાઓમાં, સંશ્લેષણ 20 પ્રમાણભૂત એમિનો એસિડનો ઉપયોગ કરે છે.
પ્રોટીન માળખું
પ્રોટીન પરમાણુઓ રેખીય પોલિમર છે જેમાં α-એમિનો એસિડનો સમાવેશ થાય છે (જે મોનોમર્સ છે) અને કેટલાક કિસ્સાઓમાં, સુધારેલા મૂળભૂત એમિનો એસિડ છે. પ્રોટીનમાં એમિનો એસિડનો ક્રમ તે પ્રોટીન માટે જનીનમાં રહેલી માહિતીને અનુરૂપ છે.
· પ્રાથમિક માળખું - પોલિપેપ્ટાઇડ સાંકળમાં એમિનો એસિડનો ક્રમ - રેખીય.
· ગૌણ માળખું એ પોલિપેપ્ટાઇડ સાંકળને હેલિક્સમાં ફેરવવાનું છે, જે હાઇડ્રોજન બોન્ડ્સ દ્વારા સપોર્ટેડ છે.
· તૃતીય માળખું - કોઇલમાં ગૌણ હેલિક્સનું પેકેજિંગ. તૃતીય માળખું જાળવો: ડાયસલ્ફાઇડ બોન્ડ, હાઇડ્રોજન બોન્ડ.
ગુણધર્મો
પ્રોટીન એ એમિનો એસિડની જેમ જ એમ્ફોટેરિક પદાર્થો છે.
તેઓ પાણીમાં દ્રાવ્યતાની ડિગ્રીમાં અલગ પડે છે, પરંતુ મોટાભાગના પ્રોટીન તેમાં ઓગળી જાય છે.
વિકૃતિકરણ: પરિસ્થિતિમાં અચાનક ફેરફાર, જેમ કે એસિડ અથવા આલ્કલી સાથે પ્રોટીનને ગરમ કરવું અથવા સારવાર કરવી, પ્રોટીન તેના ચતુર્થાંશ, તૃતીય અને ગૌણ માળખાને ગુમાવવાનું કારણ બને છે. વિકૃતિકરણ કેટલાક કિસ્સાઓમાં ઉલટાવી શકાય તેવું છે.
હાઇડ્રોલિસિસ: ઉત્સેચકોના પ્રભાવ હેઠળ, પ્રોટીન તેના ઘટક એમિનો એસિડમાં હાઇડ્રોલાઇઝ્ડ થાય છે. આ પ્રક્રિયા થાય છે, ઉદાહરણ તરીકે, પેપ્સિન અને ટ્રિપ્સિન જેવા ઉત્સેચકોના પ્રભાવ હેઠળ માનવ પેટમાં.
શરીરમાં પ્રોટીનનાં કાર્યો
ઉત્પ્રેરક કાર્ય
ઉત્સેચકો એ પ્રોટીનનું જૂથ છે જે ચોક્કસ ઉત્પ્રેરક ગુણધર્મો ધરાવે છે. ઉત્સેચકોમાં, નીચેના પ્રોટીન નોંધી શકાય છે: ટ્રિપ્સિન, પેપ્સિન, એમીલેઝ, લિપેઝ.
માળખાકીય કાર્ય
પ્રોટીન એ લગભગ તમામ પેશીઓની નિર્માણ સામગ્રી છે: સ્નાયુ, સહાયક, સંકલિત.
રક્ષણાત્મક કાર્ય
એન્ટિબોડી પ્રોટીન જે વાયરસ અને પેથોજેનિક બેક્ટેરિયાને બેઅસર કરી શકે છે .
સિગ્નલ કાર્ય
રીસેપ્ટર પ્રોટીન પડોશી કોષોમાંથી પ્રાપ્ત સિગ્નલોને સમજે છે અને પ્રસારિત કરે છે.
પરિવહન કાર્ય
હિમોગ્લોબિન ફેફસાંમાંથી અન્ય પેશીઓમાં ઓક્સિજન અને પેશીઓમાંથી ફેફસાંમાં કાર્બન ડાયોક્સાઇડ વહન કરે છે.
સંગ્રહ કાર્ય
આ પ્રોટીનમાં કહેવાતા અનામત પ્રોટીનનો સમાવેશ થાય છે, જે છોડના બીજ અને પ્રાણીના ઈંડામાં ઊર્જા અને પદાર્થના સ્ત્રોત તરીકે સંગ્રહિત થાય છે. તેઓ મકાન સામગ્રી તરીકે સેવા આપે છે.
મોટર કાર્ય
પ્રોટીન જે સંકોચનીય પ્રવૃત્તિ કરે છે તે એક્ટીન અને માયોસિન છે
ટિકિટ નંબર 18
1. સામાન્ય લાક્ષણિકતાઓઉચ્ચ-પરમાણુ સંયોજનો: રચના, માળખું, તેમના ઉત્પાદન હેઠળની પ્રતિક્રિયાઓ (પોલીઇથિલિનના ઉદાહરણનો ઉપયોગ કરીને).
ઉચ્ચ પરમાણુ વજન સંયોજનો (પોલિમર્સ) એવા પદાર્થો છે જેના મેક્રોમોલેક્યુલ્સમાં વારંવાર પુનરાવર્તિત એકમો હોય છે. તેમનું સાપેક્ષ પરમાણુ વજન કેટલાંક હજારથી લાખો સુધીનું હોઈ શકે છે.
મોનોમરઓછા પરમાણુ પદાર્થ છે જેમાંથી પોલિમર મેળવવામાં આવે છે.
માળખાકીય લિંક- પોલિમર મેક્રોમોલેક્યુલમાં અણુઓના જૂથો ઘણી વખત પુનરાવર્તિત થાય છે.
 પોલિમરાઇઝેશનની ડિગ્રી- પુનરાવર્તિત માળખાકીય એકમોની સંખ્યા.
પોલિમરાઇઝેશનની ડિગ્રી- પુનરાવર્તિત માળખાકીય એકમોની સંખ્યા.
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n
પોલિમરાઇઝેશન અને પોલિકન્ડેન્સેશન પ્રતિક્રિયાઓ દ્વારા પોલિમર મેળવી શકાય છે.
પ્રતિક્રિયાના ચિહ્નો પોલિમરાઇઝેશન:
1. કોઈ ઉપ-ઉત્પાદનોની રચના થતી નથી.
2. પ્રતિક્રિયા ડબલ અથવા ટ્રિપલ બોન્ડને કારણે થાય છે.
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n- ઇથિલિન પોલિમરાઇઝેશન પ્રતિક્રિયા - પોલિઇથિલિનની રચના.
પ્રતિક્રિયાના ચિહ્નો પોલી કન્ડેન્સેશન:
1. આડપેદાશો રચાય છે.
2. પ્રતિક્રિયા કાર્યાત્મક જૂથોને કારણે થાય છે.
ઉદાહરણ: ફિનોલ અને ફોર્માલ્ડિહાઇડમાંથી ફિનોલ-ફોર્માલ્ડિહાઇડ રેઝિનનું નિર્માણ, એમિનો એસિડમાંથી પોલિપેપ્ટાઇડ બોન્ડ. આ કિસ્સામાં, પોલિમર ઉપરાંત, એક આડપેદાશ રચાય છે - પાણી.
ઉચ્ચ-પરમાણુ સંયોજનો અન્ય સામગ્રીઓ કરતાં ચોક્કસ ફાયદા ધરાવે છે: તેઓ રીએજન્ટ્સ માટે પ્રતિરોધક છે, વર્તમાનનું સંચાલન કરતા નથી, યાંત્રિક રીતે મજબૂત અને ઓછા વજનવાળા હોય છે. ફિલ્મો, વાર્નિશ, રબર અને પ્લાસ્ટિક પોલિમરમાંથી બનાવવામાં આવે છે.
એમિનો એસિડ, પ્રોટીન અને પેપ્ટાઇડ્સનીચે વર્ણવેલ સંયોજનોના ઉદાહરણો છે. ઘણા જૈવિક રીતે સક્રિય અણુઓમાં રાસાયણિક રીતે જુદા જુદા કાર્યાત્મક જૂથો હોય છે જે એકબીજા સાથે અને એકબીજાના કાર્યાત્મક જૂથો સાથે ક્રિયાપ્રતિક્રિયા કરી શકે છે.
એમિનો એસિડ.
એમિનો એસિડ- કાર્બનિક બાયફંક્શનલ સંયોજનો, જેમાં કાર્બોક્સિલ જૂથનો સમાવેશ થાય છે - યુએનએસ, અને એમિનો જૂથ છે એન.એચ. 2 .
અલગ α અને β - એમિનો એસિડ:
મોટે ભાગે પ્રકૃતિમાં જોવા મળે છે α - એસિડ્સ. પ્રોટીનમાં 19 એમિનો એસિડ અને એક ઈમિનો એસિડ હોય છે ( C 5 H 9ના 2 ):


સૌથી સરળ એમિનો એસિડ- ગ્લાયસીન. બાકીના એમિનો એસિડને નીચેના મુખ્ય જૂથોમાં વિભાજિત કરી શકાય છે:
1) ગ્લાયસીનના હોમોલોગ્સ - એલનાઇન, વેલિન, લ્યુસીન, આઇસોલ્યુસીન.
એમિનો એસિડ મેળવવું.
એમિનો એસિડના રાસાયણિક ગુણધર્મો.
એમિનો એસિડ- આ એમ્ફોટેરિક સંયોજનો છે, કારણ કે 2 વિરોધી કાર્યાત્મક જૂથો ધરાવે છે - એક એમિનો જૂથ અને એક હાઇડ્રોક્સિલ જૂથ. તેથી, તેઓ એસિડ અને આલ્કલી બંને સાથે પ્રતિક્રિયા આપે છે:
એસિડ-બેઝ ટ્રાન્સફોર્મેશનને આ રીતે રજૂ કરી શકાય છે:
એમિનો એસિડના ગુણધર્મોરાસાયણિક અને ભૌતિક: બે જૂથોમાં વિભાજિત કરી શકાય છે.
એમિનો એસિડના રાસાયણિક ગુણધર્મો
સંયોજનો પર આધાર રાખીને, એમિનો એસિડ વિવિધ ગુણધર્મો પ્રદર્શિત કરી શકે છે.
એમિનો એસિડ ક્રિયાપ્રતિક્રિયાઓ:
એમિનો એસિડ, એમ્ફોટેરિક સંયોજનો તરીકે, એસિડ અને આલ્કલી બંને સાથે ક્ષાર બનાવે છે.
કાર્બોક્સિલિક એસિડ તરીકે, એમિનો એસિડ કાર્યાત્મક ડેરિવેટિવ્ઝ બનાવે છે: ક્ષાર, એસ્ટર, એમાઈડ્સ.
એમિનો એસિડની ક્રિયાપ્રતિક્રિયા અને ગુણધર્મો કારણો:
ક્ષાર રચાય છે:
NH 2 -CH 2 -COOH + NaOH NH 2 -CH 2 -COONa + H2O
સોડિયમ મીઠું + 2-એમિનોએસેટિક એસિડ એમિનોએસેટિક એસિડ (ગ્લાયસીન) + પાણીનું સોડિયમ મીઠું
સાથે ક્રિયાપ્રતિક્રિયા આલ્કોહોલ:
એમિનો એસિડ હાઇડ્રોજન ક્લોરાઇડ ગેસની હાજરીમાં આલ્કોહોલ સાથે પ્રતિક્રિયા કરી શકે છે, એસ્ટર. એમિનો એસિડ એસ્ટર્સ પાસે બાયપોલર માળખું નથી અને તે અસ્થિર સંયોજનો છે.
NH 2 -CH 2 -COOH + CH 3 OH NH 2 -CH 2 -COOCH 3 + H 2 O.
મિથાઈલ એસ્ટર / 2-એમિનોએસેટિક એસિડ /
ક્રિયાપ્રતિક્રિયા એમોનિયા:
એમાઈડ્સ રચાય છે:
NH 2 -CH(R)-COOH + H-NH 2 = NH 2 -CH(R)-CONH 2 + H 2 O
સાથે એમિનો એસિડની ક્રિયાપ્રતિક્રિયા મજબૂત એસિડ્સ:
અમને ક્ષાર મળે છે:
HOOC-CH 2 -NH 2 + HCl → Cl (અથવા HOOC-CH 2 -NH 2 *HCl)
આ એમિનો એસિડના મૂળભૂત રાસાયણિક ગુણધર્મો છે.
એમિનો એસિડના ભૌતિક ગુણધર્મો
ચાલો એમિનો એસિડના ભૌતિક ગુણધર્મોની યાદી કરીએ:
- રંગહીન
- સ્ફટિકીય સ્વરૂપ છે
- મોટાભાગના એમિનો એસિડનો સ્વાદ મીઠો હોય છે, પરંતુ આમૂલ (R) ના આધારે તે કડવો અથવા સ્વાદહીન હોઈ શકે છે.
- પાણીમાં સરળતાથી દ્રાવ્ય, પરંતુ ઘણા કાર્બનિક દ્રાવકોમાં નબળી રીતે દ્રાવ્ય
- એમિનો એસિડમાં ઓપ્ટિકલ પ્રવૃત્તિની મિલકત હોય છે
- 200 ° સે ઉપરના તાપમાને વિઘટન સાથે ઓગળે છે
- બિન-અસ્થિર
- એસિડિક અને આલ્કલાઇન વાતાવરણમાં એમિનો એસિડના જલીય દ્રાવણો ઇલેક્ટ્રિક પ્રવાહનું સંચાલન કરે છે









