Aminokislotalar har qanday tirik organizmning asosiy qurilish materialidir. O'z tabiatiga ko'ra, ular tuproqdan sintez qilinadigan o'simliklarning birlamchi azotli moddalari hisoblanadi. Aminokislotalarning tuzilishi ularning tarkibiga bog'liq.
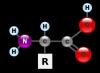
Aminokislota tuzilishi
Uning har bir molekulasi radikal bilan bog'langan karboksil va amin guruhlariga ega. Agar aminokislota 1 karboksil va 1 aminokislotadan iborat bo'lsa, uning tuzilishini quyida keltirilgan formula bilan ko'rsatish mumkin.

1 kislota va 1 ishqoriy guruhga ega bo'lgan aminokislotalarga monoaminomonokarboksilik kislotalar deyiladi. Organizmlarda 2 karboksil guruhi yoki 2 amin guruhi ham sintezlanadi va ularning vazifalari aniqlanadi. Tarkibida 2 ta karboksil va 1 ta amin guruhi boʻlgan aminokislotalar monoaminodikarboksilik, 2 ta amin va 1 ta karboksil boʻlganlari esa diaminomonokarboksilik deyiladi.
Ular organik radikal R tuzilishida ham farqlanadi. Ularning har biri oʻz nomi va tuzilishiga ega. Demak, aminokislotalarning turli funktsiyalari. Bu kislotali va gidroksidi guruhlarning mavjudligi uning yuqori reaktivligini ta'minlaydi. Bu guruhlar aminokislotalarni birlashtiradi va polimer - oqsil hosil qiladi. Proteinlar tuzilishiga ko'ra polipeptidlar deb ham ataladi.
Aminokislotalar qurilish materiallari sifatida
Protein molekulasi o'nlab yoki yuzlab aminokislotalardan iborat zanjirdir. Proteinlar aminokislotalarning tarkibi, miqdori va tartibida farqlanadi, chunki 20 ta komponentning birikmalari soni deyarli cheksizdir. Ulardan ba'zilari muhim aminokislotalarning butun tarkibiga ega, boshqalari esa bitta yoki bir nechtasiz. Tuzilishi inson organizmidagi oqsillarning funktsiyalariga o'xshash individual aminokislotalar oziq-ovqat mahsuloti sifatida ishlatilmaydi, chunki ular yomon eriydi va oshqozon-ichak trakti tomonidan parchalanmaydi. Bularga tirnoq, sochlar, mo'yna yoki patlarning oqsillari kiradi.
Aminokislotalarning funktsiyalarini ortiqcha baholash qiyin. Bu moddalar inson ratsionidagi asosiy oziq-ovqat hisoblanadi. Aminokislotalar qanday vazifani bajaradi? Ular mushak massasining o'sishini oshiradi, bo'g'inlar va ligamentlarni mustahkamlashga yordam beradi, shikastlangan tana to'qimalarini tiklaydi va inson tanasida sodir bo'ladigan barcha jarayonlarda ishtirok etadi.

Muhim aminokislotalar
Faqat qo'shimchalar yoki oziq-ovqat mahsulotlaridan sog'lom bo'g'inlarni shakllantirish jarayonida funktsiyalarni olishingiz mumkin, kuchli mushaklar, chiroyli sochlar juda muhimdir. Ushbu aminokislotalarga quyidagilar kiradi:
- fenilalanin;
- lizin;
- treonin;
- metionin;
- valin;
- leysin;
- triptofan;
- histidin;
- izolösin.
Muhim aminokislotalarning vazifalari
Ushbu g'ishtlar inson tanasining har bir hujayrasi faoliyatida muhim funktsiyalarni bajaradi. Ular tanaga etarli miqdorda kirsa, ular ko'rinmas, ammo ularning etishmasligi butun tananing ishini sezilarli darajada buzadi.
- Valin mushaklarni yangilaydi va ajoyib energiya manbai bo'lib xizmat qiladi.
- Histidin qon tarkibini yaxshilaydi, mushaklarning tiklanishi va o'sishiga yordam beradi, bo'g'inlar faoliyatini yaxshilaydi.
- Izoleysin gemoglobin ishlab chiqarishga yordam beradi. Qondagi shakar miqdorini nazorat qiladi, insonning energiyasini va chidamliligini oshiradi.
- Leysin immunitet tizimini mustahkamlaydi, qondagi shakar va leykotsitlar darajasini nazorat qiladi. Leykotsitlar darajasi juda yuqori bo'lsa: ularni pasaytiradi va yallig'lanishni bartaraf etish uchun tananing zahiralarini faollashtiradi.
- Lizin suyaklarni quradigan va mustahkamlaydigan kaltsiyni so'rishga yordam beradi. Kollagen ishlab chiqarishga yordam beradi, soch tuzilishini yaxshilaydi. Erkaklar uchun bu ajoyib anabolik steroiddir, chunki u mushaklarni quradi va erkaklar kuchini oshiradi.
- Metionin ovqat hazm qilish tizimi va jigar faoliyatini normallantiradi. Yog'larning parchalanishida ishtirok etadi, homilador ayollarda toksikozni yo'q qiladi va sochlarga foydali ta'sir ko'rsatadi.
- Treonin oshqozon-ichak trakti faoliyatini yaxshilaydi. Immunitetni oshiradi, elastin va kollagen hosil bo'lishida ishtirok etadi. Treonin jigarda yog 'birikmasini oldini oladi.
- Triptofan inson hissiyotlari uchun javobgardir. Serotonin - baxt gormoni ishlab chiqaradi, shu bilan uyquni normallantiradi va kayfiyatni ko'taradi. Ishtahani yumshatadi, yurak mushaklari va arteriyalarga foydali ta'sir ko'rsatadi.
- Fenilalanin nerv hujayralaridan boshning miyasiga signallarni uzatuvchi sifatida xizmat qiladi. Kayfiyatni yaxshilaydi, nosog'lom ishtahani bostiradi, xotirani yaxshilaydi, sezgirlikni oshiradi, og'riqni kamaytiradi.
Muhim aminokislotalarning etishmasligi o'sishning sekinlashishiga, metabolik kasalliklarga va mushak massasining pasayishiga olib keladi.

Muhim bo'lmagan aminokislotalar
Bu aminokislotalar bo'lib, ularning tuzilishi va funktsiyalari tanada ishlab chiqariladi:
- arginin;
- alanin;
- asparagin;
- glitsin;
- prolin;
- taurin;
- tirozin;
- glutamat;
- serin;
- glutamin;
- ornitin;
- sistein;
- karnitin
Muhim bo'lmagan aminokislotalarning funktsiyalari
- Sistein toksik moddalarni yo'q qiladi, teri va mushak to'qimalarini yaratishda ishtirok etadi va tabiiy antioksidantdir.
- Tirozin jismoniy charchoqni kamaytiradi, metabolizmni tezlashtiradi, stress va depressiyani yo'q qiladi.
- Alanin mushaklarning o'sishi uchun xizmat qiladi va energiya manbai hisoblanadi.
- metabolizmni oshiradi va og'ir jismoniy mashqlar paytida ammiak hosil bo'lishini kamaytiradi.
- Sistin ligamentlar va bo'g'inlar shikastlanganda og'riqni yo'q qiladi.
- miya faoliyati uchun mas'ul bo'lib, uzoq muddatli jismoniy faoliyat davomida u energiya ishlab chiqaradigan glyukozaga aylanadi.
- Glutamin mushaklarni tiklaydi, immunitetni yaxshilaydi, metabolizmni tezlashtiradi, miya faoliyatini yaxshilaydi va o'sish gormonini yaratadi.
- Glitsin mushaklarning ishlashi, yog'larning parchalanishi, qon bosimi va qon shakarini barqarorlashtirish uchun zarurdir.
- Karnitin yog 'kislotalarini hujayralarga o'tkazadi, ular energiyani chiqarish uchun parchalanadi, natijada ortiqcha yog'lar yonadi va energiya hosil bo'ladi.
- Ornitin o'sish gormonini ishlab chiqaradi, siydik hosil bo'lish jarayonida ishtirok etadi, yog' kislotalarini parchalaydi va insulin ishlab chiqarishga yordam beradi.
- Prolin kollagen ishlab chiqarishni ta'minlaydi, bu ligamentlar va bo'g'inlar uchun zarurdir.
- Serin immunitetni yaxshilaydi va energiya ishlab chiqaradi, u yog 'kislotalarining tez almashinuvi va mushaklarning o'sishi uchun zarurdir.
- Taurin yog'larni parchalaydi, tananing qarshiligini oshiradi va safro tuzlarini sintez qiladi.
Protein va uning xossalari
Proteinlar yoki oqsillar azotni o'z ichiga olgan yuqori molekulyar birikmalardir. Birinchi marta 1838 yilda Berzelius tomonidan belgilangan "oqsil" tushunchasi yunoncha so'zdan kelib chiqqan va "birlamchi" degan ma'noni anglatadi, bu oqsillarning tabiatdagi etakchi rolini aks ettiradi. Oqsillarning xilma-xilligi juda ko'p sonli tirik mavjudotlarning mavjud bo'lishiga imkon beradi: bakteriyalardan inson tanasigacha. Ularning soni boshqa makromolekulalarga qaraganda ancha ko'p, chunki oqsillar tirik hujayraning asosidir. Ular inson tanasi massasining taxminan 20% ni, hujayraning quruq massasining 50% dan ko'prog'ini tashkil qiladi. Turli xil oqsillarning bu soni yigirma xil aminokislotalarning xususiyatlari bilan izohlanadi, ular bir-biri bilan o'zaro ta'sir qiladi va polimer molekulalarini yaratadi.

Proteinlarning ajoyib xususiyati - bu ma'lum bir oqsilga xos bo'lgan ma'lum fazoviy strukturani mustaqil ravishda yaratish qobiliyati. Proteinlar peptid bog'lari bo'lgan biopolimerlardir. Proteinlarning kimyoviy tarkibi taxminan 16% ni tashkil etadigan doimiy o'rtacha azot miqdori bilan tavsiflanadi.
Hayot, shuningdek, tananing o'sishi va rivojlanishi, yangi hujayralarni qurish uchun protein aminokislotalarining funktsiyasisiz mumkin emas. Proteinlarni boshqa elementlar bilan almashtirish mumkin emas, ularning inson tanasidagi roli juda muhimdir.
Proteinlarning funktsiyalari
Proteinlarga bo'lgan ehtiyoj quyidagi funktsiyalarda yotadi:
- o'sish va rivojlanish uchun zarurdir, chunki u yangi hujayralarni yaratish uchun asosiy qurilish materialidir;
- metabolizmni boshqaradi, uning davomida energiya chiqariladi. Oziq-ovqatlarni iste'mol qilgandan so'ng, metabolizm tezligi oshadi, masalan, oziq-ovqat uglevodlardan iborat bo'lsa, metabolizm 4% ga, oqsillardan iborat bo'lsa - 30% ga tezlashadi;
- uning hidrofilligi tufayli organizmda tartibga solish - suvni jalb qilish qobiliyati;
- infektsiyadan himoya qiluvchi va kasallik tahdidini bartaraf etadigan antikorlarni sintez qilish orqali immunitet tizimini mustahkamlash.

Mahsulotlar - oqsil manbalari
Inson mushaklari va skeleti nafaqat faoliyat yuritadigan, balki hayot davomida yangilanib turadigan tirik to'qimalardan iborat. Ular zararni tiklaydilar va kuch va chidamlilikni saqlaydilar. Buning uchun ular juda aniq oziq moddalarni talab qiladi. Oziq-ovqat tanani barcha jarayonlar, jumladan, mushaklarning ishlashi, to'qimalarning o'sishi va tiklanishi uchun zarur bo'lgan energiya bilan ta'minlaydi. Organizmdagi oqsil esa energiya manbai sifatida ham, qurilish materiali sifatida ham ishlatiladi.

Shuning uchun uni oziq-ovqatda kundalik foydalanishni kuzatish juda muhimdir. Proteinga boy ovqatlar: tovuq, kurka, yog'siz jambon, cho'chqa go'shti, mol go'shti, baliq, qisqichbaqalar, loviya, yasmiq, bekon, tuxum, yong'oqlar. Bu mahsulotlarning barchasi tanani oqsil bilan ta'minlaydi va hayot uchun zarur bo'lgan energiyani ta'minlaydi.
1.Aminokislotalar namoyishi amfoter xossalari va kislotalar va aminlar, shuningdek, ushbu guruhlarning birgalikda mavjudligi sababli o'ziga xos xususiyatlar. Suvli eritmalarda AMK ichki tuzlar (bipolyar ionlar) shaklida mavjud. Monoaminomonokarboksilik kislotalarning suvli eritmalari lakmus uchun neytraldir, chunki ularning molekulalarida teng miqdordagi -NH 2 - va -COOH guruhlari mavjud. Ushbu guruhlar bir-biri bilan o'zaro ta'sirlanib, ichki tuzlarni hosil qiladi:
Bunday molekula ikki joyda qarama-qarshi zaryadga ega: musbat NH 3+ va karboksilda manfiy -COO -. Shu munosabat bilan AMK ning ichki tuzi bipolyar ion yoki Tsvitter ioni (Zwitter - gibrid) deb ataladi.
Kislotali muhitda bipolyar ion o'zini kation kabi tutadi, chunki karboksil guruhining dissotsiatsiyasi bostiriladi; ishqoriy muhitda - anion sifatida. Har bir aminokislota uchun o'ziga xos pH qiymatlari mavjud, ularda eritmadagi anionik shakllar soni katyonik shakllar soniga teng. AMK molekulasining umumiy zaryadi 0 ga teng bo'lgan pH qiymati AMK ning izoelektrik nuqtasi (pI AA) deb ataladi.
Monoaminodikarboksilik kislotalarning suvli eritmalari kislotali reaksiyaga ega:
HOOC-CH 2 -CH-COOH « - OOC-CH 2 -CH–COO - + H +
Monoaminodikarboksilik kislotalarning izoelektrik nuqtasi kislotali muhitda bo'ladi va bunday AMAlar kislotali deb ataladi.
Diaminomonokarboksilik kislotalar suvli eritmalarda asosiy xususiyatlarga ega (dissosiatsiya jarayonida suvning ishtiroki ko'rsatilishi kerak):
NH 2 -(CH 2) 4 -CH-COOH + H 2 O « NH 3 + -(CH 2) 4 -CH–COO - + OH -
Diaminomonokarboksilik kislotalarning izoelektrik nuqtasi pH>7 da bo'ladi va bunday AMAlar asosli deb ataladi.
Bipolyar ionlar bo'lgan aminokislotalar amfoter xususiyatga ega: ular kislotalar va asoslar bilan tuzlar hosil qila oladilar:
HCl xlorid kislotasi bilan o'zaro ta'sir tuz hosil bo'lishiga olib keladi:
R-CH-COOH + HCl ® R-CH-COOH
NH 2 NH 3 + Cl -
Baza bilan o'zaro ta'sir tuz hosil bo'lishiga olib keladi:
R-CH(NH 2)-COOH + NaOH ® R-CH(NH 2)-COONa + H 2 O
2. Metallar bilan komplekslar hosil qilish- xelat kompleksi. Glikolning (glisin) mis tuzining tuzilishi quyidagi formula bilan ifodalanishi mumkin:

Inson tanasida mavjud bo'lgan deyarli barcha mis (100 mg) bu barqaror tirnoq shaklidagi birikmalar shaklida oqsillar (aminokislotalar) bilan bog'langan.
3. Boshqa kislotalarga o'xshash aminokislotalar efirlar, galogen angidridlar, amidlar hosil qiladi.
4. Dekarboksillanish reaksiyalari organizmda maxsus dekarboksilaza fermentlari ishtirokida yuzaga keladi: hosil bo'lgan aminlar (triptamin, gistamin, serotinin) biogen aminlar deb ataladi va inson tanasining bir qator fiziologik funktsiyalarini tartibga soluvchidir.
5. Formaldegid bilan o'zaro ta'siri(aldegidlar)
R-CH-COOH + H 2 C=O ® R-CH-COOH
Formaldegid NH 2 guruhini bog'laydi, -COOH guruhi erkin qoladi va ishqor bilan titrlash mumkin. Shuning uchun bu reaksiya aminokislotalarni miqdoriy aniqlash uchun ishlatiladi (Sørensen usuli).
6. Azot kislotasi bilan o'zaro ta'siri gidroksi kislotalarning hosil bo'lishiga va azotning ajralib chiqishiga olib keladi. Chiqarilgan azot N2 hajmiga qarab, uning o'rganilayotgan ob'ektdagi miqdoriy miqdori aniqlanadi. Ushbu reaktsiya aminokislotalarni miqdoriy aniqlash uchun ishlatiladi (Van-Slyke usuli):
R-CH-COOH + HNO 2 ® R-CH-COOH + N 2 + H 2 O
Bu tanadan tashqarida AMKni zararsizlantirish usullaridan biridir
7. Aminokislotalarning asillanishi. AMK ning aminokislotalari xona haroratida allaqachon kislota xloridlari va angidridlari bilan asillangan bo'lishi mumkin.
Yozilgan reaksiya mahsuloti atsetil-a-aminopropion kislotadir.
AMK ning atsil hosilalari ularning oqsillardagi ketma-ketligini o'rganishda va peptidlar sintezida (aminokislotalarni himoya qilish) keng qo'llaniladi.
8.Maxsus xususiyatlar aminokislotalar va karboksil guruhlarning mavjudligi va o'zaro ta'siri bilan bog'liq reaktsiyalar - peptidlarning shakllanishi. a-AMK ning umumiy mulki hisoblanadi polikondensatsiya jarayoni, peptidlarning shakllanishiga olib keladi. Ushbu reaksiya natijasida bir AMK ning karboksil guruhi va boshqa AMK ning aminokislotalari o'rtasidagi o'zaro ta'sir joyida amid bog'lari hosil bo'ladi. Boshqacha aytganda, peptidlar aminokislotalarning aminokislotalarning aminokislotalar va karboksillarining o'zaro ta'siri natijasida hosil bo'lgan amidlardir. Bunday birikmalardagi amid bog'i peptid bog'i deyiladi (peptid guruhi va peptid bog'lanish tuzilishini tushuntiring: uch markazli p, p-konjugatsiyalangan tizim)
Molekuladagi aminokislota qoldiqlari soniga qarab di-, tri-, tetrapeptidlar va boshqalar farqlanadi. polipeptidlargacha (100 tagacha AMK qoldiqlari). Oligopeptidlar 2 dan 10 gacha AMK qoldiqlarini o'z ichiga oladi, oqsillar 100 dan ortiq AMK qoldiqlarini o'z ichiga oladi Umuman olganda, polipeptid zanjiri diagramma bilan ifodalanishi mumkin:
H 2 N-CH-CO-NH-CH-CO-NH-CH-CO-... -NH-CH-COOH
Bu erda R 1, R 2, ... R n aminokislotalar radikallari.
Proteinlar haqida tushuncha.
Aminokislotalarning eng muhim biopolimerlari oqsillar - oqsillardir. Inson tanasida 5 millionga yaqin mavjud. teri, mushaklar, qon va boshqa to'qimalarni tashkil etuvchi turli xil oqsillar. Proteinlar (oqsillar) o'z nomini yunoncha "protos" so'zidan oladi - birinchidan, eng muhimi. Oqsillar organizmda bir qancha muhim vazifalarni bajaradi: 1. Qurilish funktsiyasi; 2. Transport funktsiyasi; 3. Himoya funktsiyasi; 4. Katalitik funksiya; 5. Gormonal funktsiya; 6. Oziqlanish funktsiyasi.
Barcha tabiiy oqsillar aminokislotalar monomerlaridan hosil bo'ladi. Oqsillar gidrolizlanganda AMK aralashmasi hosil bo'ladi. Ushbu AMKlarning 20 tasi mavjud.
4. Tasviriy material: taqdimot
5. Adabiyot:
Asosiy adabiyotlar:
1. Bioorganik kimyo: darslik. Tyukavkina N.A., Baukov Yu.I. 2014 yil
- Seytembetov T.S. Kimyo: darslik - Olmaota: EVERO LLP, 2010. - 284 b.
- Bolysbekova S. M. Biogen elementlar kimyosi: darslik - Semey, 2012. - 219 b. : loy
- Verentsova L.G. Noorganik, fizik va kolloid kimyo: darslik - Almati: Evero, 2009. - 214 b. : kasal.
- Fizikaviy va kolloid kimyo / A.P.Belyaev tomonidan tahrirlangan - M.: GEOTAR MEDIA, 2008
- Verentseva L.G. Noorganik, fizik va kolloid kimyo, (tekshirish testlari) 2009 yil
Qo'shimcha adabiyotlar:
- Ravich-Scherbo M.I., Novikov V.V. Fizikaviy va kolloid kimyo. M. 2003 yil.
2. Slesarev V.I. Kimyo. Tirik kimyo asoslari. Sankt-Peterburg: Ximizdat, 2001 y
3. Ershov Yu.A. Umumiy kimyo. Biofizik kimyo. Biogen elementlar kimyosi. M.: VSh, 2003 yil.
4. Asanboeva R.D., Ilyasova M.I. Biologik muhim organik birikmalarning tuzilishi va reaktivligining nazariy asoslari. Olmaota, 2003 yil.
- Bioorganik kimyo bo'yicha laboratoriya mashg'ulotlari uchun qo'llanma, ed. USTIDA. Tyukavkina. M., Bustard, 2003 yil.
- Glinka N.L. Umumiy kimyo. M., 2003 yil.
- Ponomarev V.D. Analitik kimyo 1-qism, 2 2003 yil
6. Test savollari (teskari aloqa):
1. Polipeptid zanjirining butun tuzilishini nima belgilaydi?
2. Oqsil denaturatsiyasi nimaga olib keladi?
3. Izoelektrik nuqta nima deyiladi?
4. Qanday aminokislotalar muhim deb ataladi?
5. Bizning tanamizda oqsillar qanday hosil bo'ladi?
Tegishli ma'lumotlar.
Aminokislotalar organik amfoter birikmalardir. Ular molekulada qarama-qarshi tabiatning ikkita funktsional guruhini o'z ichiga oladi: asosiy xususiyatlarga ega bo'lgan aminokislotalar va kislotali xususiyatlarga ega bo'lgan karboksil guruhi. Aminokislotalar ham kislotalar, ham asoslar bilan reaksiyaga kirishadi:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
Aminokislotalar suvda eritilganda, karboksil guruhi aminokislotalar bilan birikishi mumkin bo'lgan vodorod ionini chiqaradi. Bunday holda, molekulasi bipolyar ion bo'lgan ichki tuz hosil bo'ladi:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO -.
Aminokislotalarning turli muhitlarda kislota-asos o'zgarishini quyidagi umumiy diagramma bilan ifodalash mumkin:

Aminokislotalarning suvli eritmalari funktsional guruhlar soniga qarab neytral, ishqoriy yoki kislotali muhitga ega. Shunday qilib, glutamik kislota kislotali eritma hosil qiladi (ikkita -COOH guruhi, bitta -NH 2), lizin ishqoriy eritma hosil qiladi (bitta -COOH guruhi, ikkita -NH 2).
Birlamchi aminlar singari, aminokislotalar azot kislotasi bilan reaksiyaga kirishadi, aminokislotalar gidrokso guruhiga va aminokislota gidroksi kislotaga aylanadi:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
Chiqarilgan azot hajmini o'lchash bizga aminokislota miqdorini aniqlash imkonini beradi ( Van Slayk usuli).
Aminokislotalar vodorod xlorid gazi ishtirokida spirtli ichimliklar bilan reaksiyaga kirishib, efirga (aniqrog'i, esterning gidroxlorid tuzi) aylanadi:
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + H 2 O.
Aminokislota efirlari bipolyar tuzilishga ega emas va uchuvchan birikmalardir.
Aminokislotalarning eng muhim xususiyati ularning peptidlar hosil qilish uchun kondensatsiyalanish qobiliyatidir.
Sifatli reaksiyalar.
1) Barcha aminokislotalar ningidrin bilan oksidlanadi

ko'k-binafsha rangli mahsulotlarning shakllanishi bilan. Iminokislota prolini ningidrin bilan sariq rang beradi. Bu reaksiya spektrofotometriya yordamida aminokislotalarning miqdorini aniqlash uchun ishlatilishi mumkin.
2) Aromatik aminokislotalar konsentrlangan nitrat kislota bilan qizdirilganda benzol halqasining nitrlanishi sodir bo'ladi va sariq rangli birikmalar hosil bo'ladi. Bu reaksiya deyiladi ksantoprotein(yunoncha xanthos - sariq).
Barcha a-aminokislotalar, glitsindan tashqari, chiral a-uglerod atomini o'z ichiga oladi va ular quyidagicha paydo bo'lishi mumkin. enantiomerlar:
Deyarli barcha tabiiy aminokislotalar -uglerod atomida bir xil nisbiy konfiguratsiyaga ega ekanligi ko'rsatilgan. -(-)-serinning uglerod atomi shartli ravishda tayinlangan L-konfiguratsiya va -(+)-serinning uglerod atomi - D-konfiguratsiya. Bundan tashqari, agar aminokislotalarning Fisher proyeksiyasi shunday yozilsa, karboksil guruhi tepada va R pastda joylashgan bo'lsa, u holda L-aminokislotalar, amino guruhi chap tomonda bo'ladi va D- aminokislotalar - o'ngda. Fisherning aminokislotalar konfiguratsiyasini aniqlash sxemasi chiral a-uglerod atomiga ega bo'lgan barcha a-aminokislotalar uchun amal qiladi.
Rasmdan ko'rinib turibdiki L-aminokislota radikalning tabiatiga ko'ra dekstrorotator (+) yoki levorotator (-) bo'lishi mumkin. Tabiatda mavjud bo'lgan aminokislotalarning katta qismi L- qator. Ularning enantiomorflar, ya'ni. D-aminokislotalar faqat mikroorganizmlar tomonidan sintezlanadi va deyiladi "g'ayritabiiy" aminokislotalar.
(R,S) nomenklaturasiga ko'ra, ko'pchilik "tabiiy" yoki L-aminokislotalar S konfiguratsiyasiga ega.
L-izoleysin va L-treonin, har bir molekulada ikkita chiral markazdan iborat bo'lib, -uglerod atomidagi konfiguratsiyaga qarab, diastereomerlar juftligining istalgan a'zosi bo'lishi mumkin. Ushbu aminokislotalarning to'g'ri mutlaq konfiguratsiyasi quyida keltirilgan.
aminokislotalarning kislota-asosli xossalari
Aminokislotalar amfoter moddalar bo'lib, ular kationlar yoki anionlar shaklida mavjud bo'lishi mumkin. Bu xususiyat ikkala kislotali ( -KOUN) va asosiy ( -NH 2 ) bir molekuladagi guruhlar. Juda kislotali eritmalarda N.H. 2 Kislota guruhi protonlanadi va kislota kationga aylanadi. Kuchli ishqoriy eritmalarda aminokislotalarning karboksil guruhi deprotonlanadi va kislota anionga aylanadi.
Qattiq holatda aminokislotalar shaklda mavjud zvitterionlar (bipolyar ionlar, ichki tuzlar). Tsvitterionlarda proton karboksil guruhidan aminokislotalarga o'tadi:
Agar siz aminokislotani o'tkazuvchan muhitga joylashtirsangiz va u erda bir juft elektrodni tushirsangiz, kislotali eritmalarda aminokislotalar katodga, ishqoriy eritmalarda esa anodga o'tadi. Berilgan aminokislotaga xos bo'lgan ma'lum bir pH qiymatida u anodga ham, katodga ham o'tmaydi, chunki har bir molekula zvitterion shaklida bo'ladi (ham musbat, ham manfiy zaryadga ega). Ushbu pH qiymati deyiladi izoelektrik nuqta(pI) berilgan aminokislota.
AMINOKISLATLARNING REAKSIYALARI
Aminokislotalarning laboratoriyada o'tkazadigan reaktsiyalarining aksariyati ( in vitro), barcha aminlar yoki karboksilik kislotalarga xosdir.
1. karboksil guruhida amidlarning hosil bo'lishi. Aminokislotalarning karbonil guruhi aminning aminokislotalari bilan reaksiyaga kirishganda, aminokislotalarning polikondensatlanish reaksiyasi parallel ravishda sodir bo‘lib, amidlar hosil bo‘lishiga olib keladi. Polimerizatsiyani oldini olish uchun kislotaning aminokislotalari bloklanadi, shunda faqat aminning amino guruhi reaksiyaga kirishadi. Shu maqsadda karbobenzoksixlorid (karbobenziloksixlorid, benzilxloroformat) ishlatiladi. ishqalaydi-butoksikarboksazid va boshqalar. Omin bilan reaksiyaga kirishish uchun karboksil guruhi etilxloroformat bilan ishlov berish orqali faollashadi. Himoya guruhi keyin katalitik gidrogenoliz yoki vodorod bromidning sirka kislotasidagi sovuq eritmasi ta'sirida chiqariladi.

2. aminokislotalarda amidlarning hosil bo'lishi. Aminokislotalarning aminokislotalarini asillanganda amid hosil bo'ladi.

Reaksiya asosiy muhitda yaxshiroq davom etadi, chunki bu erkin aminning yuqori konsentratsiyasini ta'minlaydi.
3. efirlarning hosil bo'lishi. Aminokislotalarning karboksil guruhi an'anaviy usullar bilan oson esterlanadi. Masalan, metil efirlari quruq vodorod xlorid gazini metanoldagi aminokislota eritmasidan o‘tkazish yo‘li bilan tayyorlanadi:

Aminokislotalar polikondensatsiyaga qodir, natijada poliamid hosil bo'ladi. -aminokislotalardan tashkil topgan poliamidlar deyiladi peptidlar yoki polipeptidlar . Bunday polimerlardagi amid bog'lanish deyiladi peptid aloqa. Molekulyar og'irligi kamida 5000 bo'lgan polipeptidlar deyiladi oqsillar . Proteinlar taxminan 25 xil aminokislotalarni o'z ichiga oladi. Berilgan oqsil gidrolizlanganda, bu aminokislotalarning barchasi yoki ularning bir qismi alohida oqsilga xos bo'lgan ma'lum nisbatlarda hosil bo'lishi mumkin.
Berilgan oqsilga xos bo'lgan zanjirdagi aminokislotalar qoldiqlarining noyob ketma-ketligi deyiladi asosiy protein tuzilishi . Protein molekulalarining burilish zanjirlarining xususiyatlari (kosmosda bo'laklarning o'zaro joylashishi) deyiladi. oqsillarning ikkilamchi tuzilishi . Oqsillarning polipeptid zanjirlari aminokislotalar yon zanjirlari hisobiga amid, disulfid, vodorod va boshqa aloqalarni hosil qilish uchun bir-biriga bog'lanishi mumkin. Natijada, spiral to'pga aylanadi. Ushbu strukturaviy xususiyat deyiladi oqsilning uchinchi darajali tuzilishi . Biologik faollikni ko'rsatish uchun ba'zi oqsillar birinchi navbatda makrokompleks hosil qilishi kerak ( oligoprotein), bir nechta to'liq oqsil bo'linmalaridan iborat. To'rtlamchi tuzilish biologik faol materialda bunday monomerlarning assotsiatsiyasi darajasini aniqlaydi.
Proteinlar ikkita katta guruhga bo'linadi - fibrillar (molekula uzunligining eniga nisbati 10 dan katta) va sharsimon (nisbat 10 dan kam). Fibrillyar oqsillarga kiradi kollagen , umurtqali hayvonlarda eng ko'p protein; u xaftaga quruq og'irligining deyarli 50% va suyakning qattiq moddasining taxminan 30% ni tashkil qiladi. O'simliklar va hayvonlarning aksariyat tartibga solish tizimlarida kataliz globulyar oqsillar tomonidan amalga oshiriladi, ular deyiladi. fermentlar .
Aminokislotalarning kislota-ishqor xossalari ularning tarkibida ikkita ionlashtiriladigan guruh - karboksil va aminokislotalar mavjudligi bilan bog'liq, shuning uchun aminokislotalar ham kislotalar, ham asoslarning xususiyatlarini namoyon qilishi mumkin, ya'ni. ular amfoter birikmalardir. Kristal holatida va suvli eritmalarda a-aminokislotalar bipolyar ionlar shaklida mavjud bo'lib, ular zvitterionlar deb ham ataladi. Ion tuzilishi a-aminokislotalarning ayrim xossalarini belgilaydi: yuqori erish nuqtasi (200-300°C), uchuvchan emasligi, suvda eruvchanligi va qutbsiz organik erituvchilarda erimasligi. Aminokislotalarning suvda eruvchanligi ularning organizmda so‘rilishi va tashilishi bilan bog‘liq. Aminokislotalar molekulalarining ionlanishi eritmaning pH ga bog'liq. Monoaminomonokarboksilik kislotalar uchun dissotsilanish jarayoni quyidagi shaklga ega:
Kuchli kislotali eritmalarda aminokislotalar musbat ionlar, ishqoriy eritmalarda esa manfiy ionlar shaklida bo’ladi.
Aminokislotalarning kislota-asos xossalarini Bronsted-Lowrining kislotalar va asoslar nazariyasiga asoslanib tushuntirish mumkin. Bronsted nazariyasi nuqtai nazaridan to'liq protonlangan -aminokislota (kationik shakl) ikki kislotali guruhni o'z ichiga olgan ikki asosli kislotadir: dissotsilanmagan karboksil guruhi (- COOH) va protonlangan aminokislotalar (NH 3), ular xarakterlanadi. pK 1 va pK 2 ning mos qiymatlari bo'yicha.
Aminokislotalar uchun pK qiymatlari titrlash egri chizig'idan aniqlanadi. Alaninning titrlash egri chizig'ini ko'rib chiqaylik (1-rasm).

Guruch. 1 – 0,1 M alanin eritmasini 0,1 M HCl eritmasi (a) va 0,1 M NaOH eritmasi (b) bilan titrlash natijasida olingan egri chiziqlar.
Alaninning titrlash egri chizig'idan ko'rinadiki, karboksil guruhi pK 1 = 2,34, protonlangan aminokislota guruhi esa pK 2 = 9,69 ga ega. PH = 6,02 da, zarrachaning umumiy elektr zaryadi 0 bo'lsa, alanin bipolyar ion sifatida mavjud. Ushbu pH qiymatida alanin molekulasi elektr neytral hisoblanadi. Ushbu pH qiymati izoelektrik nuqta deb ataladi va pH et yoki pI bilan belgilanadi. Monoaminomonokarboksilik kislotalar uchun izoelektrik nuqta ikkita pK qiymatining o'rtacha arifmetik qiymati sifatida hisoblanadi. Masalan, alanin uchun u quyidagilarga teng:
rI= ½(rK 1 + rK 2) = ½(2,34 + 9,69) = 6,02
Izoelektrik nuqtadan yuqori pH qiymatida aminokislota manfiy zaryadlanadi va pI dan past pH qiymatida aminokislota aniq musbat zaryad oladi. Masalan, pH = 1,0 da barcha alanin molekulalari ionlar shaklida mavjud

umumiy to'lov bilan +1. pH = 2,34 da, teng miqdordagi ionlar aralashmasi mavjud bo'lganda

umumiy to'lov = +0,5. Xuddi shunday, har qanday pH qiymatida boshqa har qanday amino kislotalar uchun umumiy zaryadning belgisi va kattaligini taxmin qilishingiz mumkin.
Radikalda ionlanadigan guruhga ega bo'lgan aminokislotalar ionlanishning uchta mumkin bo'lgan bosqichiga to'g'ri keladigan 3 qismdan iborat bo'lgan yanada murakkab titrlash egri chiziqlariga ega va shuning uchun ular uchta pK qiymatiga ega (pK 1, pK 2 va pK) R). Aspartik kislota kabi kislotali aminokislotalarning ionlanishi quyidagi ketma-ket bosqichlardan iborat:

Bunday aminokislotalarning izoelektrik nuqtalari -aminokislotalar va -karboksil guruhlari bilan bir qatorda radikalning ionlanadigan guruhining mavjudligi bilan ham aniqlanadi. Monoaminodikarboksilik kislotalar uchun izoelektrik nuqtalar kislotali pH mintaqasiga siljiydi va ikkita karboksil guruhi uchun pK qiymatlari orasidagi o'rtacha arifmetik sifatida aniqlanadi (pIaspartik kislota = 2,97). Asosiy aminokislotalar uchun pI ishqoriy hududga o'tkaziladi va ikkita protonlangan aminokislotalar uchun pK qiymatlari orasidagi o'rtacha arifmetik sifatida hisoblanadi (pIlizin = 9,74).
Aminokislotalarning kislota-ishqor xossalari aminokislotalarni elektroforez va ion almashinish xromatografiyasi yordamida ajratish va keyinchalik aniqlash uchun ishlatiladi. Ushbu usullarning ikkalasi ham ma'lum bir pH qiymatida umumiy elektr zaryadining belgisi va kattaligidagi farqlarga asoslanadi.