Aminokislotalar organik amfoter birikmalardir. Ular molekulada qarama-qarshi tabiatning ikkita funktsional guruhini o'z ichiga oladi: asosiy xususiyatlarga ega bo'lgan aminokislotalar va kislotali xususiyatlarga ega bo'lgan karboksil guruhi. Aminokislotalar ham kislotalar, ham asoslar bilan reaksiyaga kirishadi:
H 2 N -CH 2 -COOH + HCl → Cl [H 3 N-CH 2 -COOH],
H 2 N -CH 2 -COOH + NaOH → H 2 N-CH 2 -COONa + H 2 O.
Aminokislotalar suvda eritilganda, karboksil guruhi aminokislotalar bilan birikishi mumkin bo'lgan vodorod ionini chiqaradi. Bunday holda, molekulasi bipolyar ion bo'lgan ichki tuz hosil bo'ladi:
H 2 N-CH 2 -COOH + H 3 N -CH 2 -COO –.
Aminokislotalarning turli muhitlarda kislota-asos o'zgarishini quyidagi umumiy diagramma bilan ifodalash mumkin:
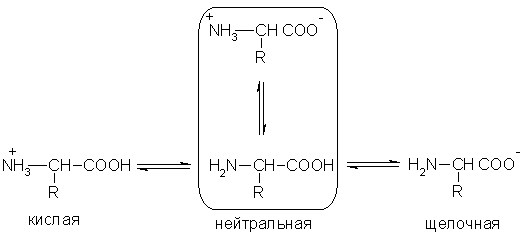
Aminokislotalarning suvli eritmalari funktsional guruhlar soniga qarab neytral, ishqoriy yoki kislotali muhitga ega. Shunday qilib, glutamik kislota kislotali eritma hosil qiladi (ikkita -COOH guruhi, bitta -NH 2), lizin ishqoriy eritma hosil qiladi (bitta -COOH guruhi, ikkita -NH 2).
Birlamchi aminlar singari, aminokislotalar azot kislotasi bilan reaksiyaga kirishadi, aminokislotalar gidrokso guruhiga va aminokislota gidroksi kislotaga aylanadi:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
Chiqarilgan azot hajmini o'lchash bizga aminokislota miqdorini aniqlash imkonini beradi ( Van Slayk usuli).
Aminokislotalar vodorod xlorid gazi ishtirokida spirtli ichimliklar bilan reaksiyaga kirishib, efirga (aniqrog'i, esterning gidroxlorid tuzi) aylanadi:
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + H 2 O.
Aminokislota efirlari bipolyar tuzilishga ega emas va uchuvchan birikmalardir.
Aminokislotalarning eng muhim xususiyati ularning peptidlar hosil qilish uchun kondensatsiyalanish qobiliyatidir.
Sifatli reaksiyalar.
1) Barcha aminokislotalar ningidrin bilan oksidlanadi

ko'k-binafsha rangli mahsulotlarning shakllanishi bilan. Iminokislota prolini ningidrin bilan sariq rang beradi. Bu reaksiya spektrofotometriya yordamida aminokislotalarning miqdorini aniqlash uchun ishlatilishi mumkin.
2) Aromatik aminokislotalar konsentrlangan nitrat kislota bilan qizdirilganda benzol halqasining nitrlanishi sodir bo'ladi va sariq rangli birikmalar hosil bo'ladi. Bu reaksiya deyiladi ksantoprotein(yunoncha xanthos - sariq).
Barcha tabiiy aminokislotalarni quyidagi asosiy guruhlarga bo'lish mumkin:
1) alifatik to'yingan aminokislotalar(glisin, alanin);
2) oltingugurt o'z ichiga olgan aminokislotalar(sistein);
3) alifatik gidroksil guruhi bo'lgan aminokislotalar(serin);
4) aromatik aminokislotalar(fenilalanin, tirozin);
5) kislota radikali bo'lgan aminokislotalar(glutamik kislota);
6) asosiy radikal bilan aminokislotalar(lizin).
Izomerizm. Barcha a-aminokislotalarda, glisindan tashqari, a-uglerod atomi to'rt xil o'rinbosar bilan bog'langan, shuning uchun bu barcha aminokislotalar bir-birining oyna tasviri bo'lgan ikkita izomer shaklida mavjud bo'lishi mumkin.
Kvitansiya. 1. Oqsillarning gidrolizi odatda aminokislotalarning murakkab aralashmalarini hosil qiladi. Shu bilan birga, murakkab aralashmalardan individual sof aminokislotalarni olish imkonini beruvchi bir qator usullar ishlab chiqilgan.
2. Galogenni aminokislota bilan almashtirish tegishli halogen kislotalarda. Aminokislotalarni olishning bu usuli alkanlar va ammiakning halogen hosilalaridan aminlarni olish bilan mutlaqo o'xshashdir:
Jismoniy xususiyatlar. Aminokislotalar qattiq kristall moddalar bo'lib, suvda yaxshi eriydi va organik erituvchilarda ozgina eriydi. Ko'pgina aminokislotalar shirin ta'mga ega. Ular eriydi yuqori haroratlar va odatda jarayonda parchalanadi. Ular bug 'holatiga kira olmaydi.
Kimyoviy xossalari. Aminokislotalar organik amfoter birikmalardir. Ular molekulada qarama-qarshi tabiatning ikkita funktsional guruhini o'z ichiga oladi: asosiy xususiyatlarga ega bo'lgan aminokislotalar va kislotali xususiyatlarga ega bo'lgan karboksil guruhi. Aminokislotalar ham kislotalar, ham asoslar bilan reaksiyaga kirishadi:
Aminokislotalar suvda eritilganda, karboksil guruhi aminokislotalar bilan birikishi mumkin bo'lgan vodorod ionini chiqaradi. Bu yaratadi ichki tuz, molekulasi bipolyar ion bo'lgan:
Turli muhitlarda aminokislotalarning kislota-asos o'zgarishini quyidagi diagramma bilan ifodalash mumkin:
Aminokislotalarning suvli eritmalari funktsional guruhlar soniga qarab neytral, ishqoriy yoki kislotali muhitga ega. Shunday qilib, glutamik kislota kislotali eritma hosil qiladi (ikkita -COOH guruhi, bitta -NH 2), lizin ishqoriy eritma hosil qiladi (bitta -COOH guruhi, ikkita -NH 2).
Aminokislotalar vodorod xlorid gazi ishtirokida spirtlar bilan reaksiyaga kirishib, efir hosil qilishi mumkin:
Aminokislotalarning eng muhim xususiyati ularning peptidlar hosil qilish uchun kondensatsiyalanish qobiliyatidir.
Peptidlar. Peptidlar. ikki yoki undan ortiq aminokislota molekulalarining kondensatsiya mahsulotidir. Ikki aminokislota molekulasi suv molekulasini yo'q qilish uchun bir-biri bilan reaksiyaga kirishishi va parchalar bog'langan mahsulot hosil qilishi mumkin. peptid aloqasi-CO-NH-.
Olingan birikma dipeptid deb ataladi. Dipeptid molekulasi, aminokislotalar kabi, aminokislotalar va karboksil guruhini o'z ichiga oladi va yana bitta aminokislota molekulasi bilan reaksiyaga kirishishi mumkin:
Reaksiya mahsuloti tripeptid deyiladi. Peptid zanjirini ko'paytirish jarayoni printsipial jihatdan cheksiz davom etishi mumkin (polikondensatsiya) va juda yuqori molekulyar og'irlikdagi moddalarga (oqsillar) olib kelishi mumkin.
Peptidlarning asosiy xususiyati gidrolizlanish qobiliyatidir. Gidroliz jarayonida peptid zanjirining to'liq yoki qisman bo'linishi sodir bo'ladi va zanjirni tashkil etuvchi molekulyar og'irligi pastroq bo'lgan qisqaroq peptidlar yoki a-aminokislotalar hosil bo'ladi. To'liq gidroliz mahsulotlarini tahlil qilish peptidning aminokislotalar tarkibini aniqlashga imkon beradi. Peptid konsentrlangan xlorid kislota bilan uzoq vaqt qizdirilganda to'liq gidroliz sodir bo'ladi.
Peptidlarning gidrolizi kislotali yoki ishqoriy muhitda, shuningdek, fermentlar ta'sirida sodir bo'lishi mumkin. Aminokislota tuzlari kislotali va ishqoriy muhitda hosil bo'ladi:
Enzimatik gidroliz muhim ahamiyatga ega, chunki u sodir bo'ladi tanlab, T . e) peptid zanjirining qat'iy belgilangan bo'limlarini parchalashga imkon beradi.
Aminokislotalarga sifatli reaksiyalar. 1) Barcha aminokislotalar oksidlanadi ningidrin ko'k-binafsha rangli mahsulotlarning shakllanishi bilan. Bu reaksiya spektrofotometriya yordamida aminokislotalarning miqdorini aniqlash uchun ishlatilishi mumkin. 2) Aromatik aminokislotalar konsentrlangan nitrat kislota bilan qizdirilganda benzol halqasining nitrlanishi sodir bo'ladi va sariq rangli birikmalar hosil bo'ladi. Bu reaksiya deyiladi ksantoprotein(yunon tilidan ksantos - sariq).
Sincaplar. Proteinlar tabiiy polipeptidlardir yuqori qiymatlar molekulyar og'irlik (10 000 dan o'n milliongacha). Ular barcha tirik organizmlarning bir qismi bo'lib, turli xil biologik funktsiyalarni bajaradilar.
Tuzilishi. Polipeptid zanjirining tuzilishida to'rt darajani ajratish mumkin. Proteinning birlamchi tuzilishi polipeptid zanjiridagi aminokislotalarning o'ziga xos ketma-ketligidir. Peptid zanjiri faqat oz sonli oqsillarda chiziqli tuzilishga ega. Aksariyat oqsillarda peptid zanjiri fazoda ma'lum tarzda buklangan.
Ikkilamchi struktura - bu polipeptid zanjirining konformatsiyasi, ya'ni NH va CO guruhlari orasidagi vodorod aloqalari tufayli zanjirning fazoda burish usuli. Zanjirni yotqizishning asosiy usuli - bu spiral.
Proteinning uchinchi darajali tuzilishi kosmosdagi buralgan spiralning uch o'lchovli konfiguratsiyasidir. Uchinchi darajali struktura polipeptid zanjirining turli joylarida joylashgan sistein qoldiqlari orasidagi disulfid ko'priklar -S-S- tufayli hosil bo'ladi. Uchinchi darajali tuzilmaning shakllanishida ham ishtirok etadi ionli o'zaro ta'sirlar qarama-qarshi zaryadlangan guruhlar NH 3 + va COO- va hidrofobik o'zaro ta'sirlar, ya'ni, hidrofobik uglevodorod qoldiqlari strukturaning ichida bo'lishi uchun oqsil molekulasining katlanma tendentsiyasi.
Uchinchi tuzilish oqsillarning fazoviy tashkil etilishining eng yuqori shaklidir. Biroq, ba'zi oqsillar (masalan, gemoglobin) mavjud turli polipeptid zanjirlari orasidagi o'zaro ta'sir natijasida hosil bo'lgan to'rtlamchi tuzilish.
Jismoniy xususiyatlar oqsillar juda xilma-xil bo'lib, ularning tuzilishi bilan belgilanadi. Jismoniy xususiyatlariga ko'ra oqsillar ikki sinfga bo'linadi: globulyar oqsillar suvda eriydi yoki kolloid eritmalar hosil qiladi; fibrillyar oqsillar suvda erimaydi.
Kimyoviy xossalari. 1 . Oqsilning ikkilamchi va uchinchi darajali strukturasining birlamchi strukturasini saqlab qolgan holda buzilishi denaturatsiya deyiladi . Bu qizdirilganda, atrof-muhitning kislotaliligi o'zgarganda yoki radiatsiya ta'sirida paydo bo'ladi. Tuxum qaynatilganda tuxum oqining koagulyatsiyasi denaturatsiyaga misol bo'la oladi. Denaturatsiya qaytar yoki qaytarilmas bo'lishi mumkin. Qaytarib bo'lmaydigan denaturatsiya oqsillarga og'ir metallar - qo'rg'oshin yoki simob tuzlari ta'sirida erimaydigan moddalar hosil bo'lishi mumkin.
2. Protein gidrolizi - aminokislotalar hosil bo'lishi bilan kislotali yoki gidroksidi eritmada birlamchi strukturaning qaytarilmas yo'q qilinishi. Gidroliz mahsulotlarini tahlil qilib, oqsillarning miqdoriy tarkibini aniqlash mumkin.
3. Proteinlar uchun bir nechtasi ma'lum sifatli reaktsiyalar. Peptid bog'i bo'lgan barcha birikmalar ishqoriy eritmada mis (II) tuzlari ta'sirida binafsha rang beradi. Bu reaksiya deyiladi biuret. Aromatik aminokislota qoldiqlari (fenilalanin, tirozin) bo'lgan oqsillar konsentrlangan nitrat kislota ta'sirida sariq rang beradi. (ksantoprotein reaktsiya).
Oqsillarning biologik ahamiyati:
1. Tanadagi mutlaqo barcha kimyoviy reaktsiyalar katalizatorlar ishtirokida sodir bo'ladi - fermentlar. Barcha ma'lum fermentlar oqsil molekulalari. Proteinlar juda kuchli va selektiv katalizatorlardir. Ular reaktsiyalarni millionlab marta tezlashtiradi va har bir reaksiya o'zining yagona fermentiga ega.
2. Ba'zi oqsillar transport funktsiyalarini bajaradi va molekulalar yoki ionlarni sintez yoki to'planish joylariga olib boradi. Masalan, qon tarkibidagi oqsil gemoglobin kislorodni to'qimalarga va oqsilga olib boradi miyoglobin mushaklarda kislorodni saqlaydi.
3. Proteinlar qurilish materiali hujayralar. Ulardan qo'llab-quvvatlovchi, mushak va integumental to'qimalar quriladi.
4. Proteinlar muhim rol o'ynaydi immun tizimi tanasi. Maxsus oqsillar mavjud (antikorlar), begona jismlarni - viruslarni, bakteriyalarni, begona hujayralarni tanib, bog'lashga qodir.
5. Retseptor oqsillari qo'shni hujayralardan yoki ulardan keladigan signallarni qabul qiladi va uzatadi muhit. Masalan, yorug'likning ko'zning to'r pardasiga ta'siri fotoreseptor rhodopsin tomonidan seziladi. Asetilkolin kabi past molekulyar og'irlikdagi moddalar tomonidan faollashtirilgan retseptorlar nerv impulslarini nerv hujayralarining birlashmalarida uzatadi.
Yuqoridagi oqsillarning funktsiyalari ro'yxatidan ko'rinib turibdiki, oqsillar har qanday organizm uchun juda muhim va shuning uchun ular eng muhim hisoblanadi. ajralmas qismi oziq-ovqat mahsulotlari. Ovqat hazm qilish jarayonida oqsillar aminokislotalarga gidrolizlanadi, ular ma'lum bir organizm uchun zarur bo'lgan oqsillarni sintez qilish uchun boshlang'ich material bo'lib xizmat qiladi. Tana o'zini sintez qila olmaydigan va ularni faqat oziq-ovqat bilan oladigan aminokislotalar mavjud. Ushbu aminokislotalar deyiladi almashtirib bo'lmaydigan.
Leksiya: Umumiy ma'lumot polimerlar va ularning tasnifi haqida.
Aminokislotalar molekulasida aminokislotalar va karboksil guruhini o'z ichiga olgan birikmalardir. Aminokislotalarning eng oddiy vakili aminoasetik (glisin) kislota: NH 2 -CH 2 -COOH
Aminokislotalar ikkita funktsional guruhni o'z ichiga olganligi sababli, ularning xususiyatlari atomlarning ushbu guruhlariga bog'liq: NH 2 - va -COOH. Aminokislotalar amfoterdir organik moddalar, asos va kislota sifatida reaksiyaga kirishadi.
Jismoniy xususiyatlar.
Aminokislotalar rangsiz kristall moddalar bo'lib, suvda yaxshi eriydi va organik erituvchilarda ozgina eriydi. Ko'pgina aminokislotalar shirin ta'mga ega.
Kimyoviy xossalari
Kislotalar (asosiy xususiyatlar paydo bo'ladi)
Asoslar
+metall oksidlariAminokislotalar - peptidlarning hosil bo'lishi
Aminokislotalar, agar aminokislotalar va karboksil guruhlar soni bir xil bo'lsa, indikator rangini o'zgartirmaydi.
1) NH 2 -CH 2 -COOH + HCl → NH 3 Cl-CH 2 -COOH
2) NH 2 -CH 2 -COOH + NaOH → NH 2 -CH 2 -COONa + H 2 O
3) NH 2 -CH 2 -COOH + NH 2 -CH 2 -COOH → NH 2 -CH 2 -CO NH-CH 2 -COOH + H 2 O
Aminokislotalarning biologik roli shundaki, oqsilning birlamchi tuzilishi ularning qoldiqlaridan hosil bo'ladi. Bizning tanamizda oqsillarni ishlab chiqarish uchun boshlang'ich materiallar bo'lgan 20 ta aminokislotalar mavjud. Ba'zi aminokislotalar terapevtik vositalar sifatida ishlatiladi, masalan, glutamik kislota - asab kasalliklari uchun, histidin - oshqozon yarasi uchun. Ba'zi aminokislotalar oziq-ovqat sanoatida qo'llaniladi, ular oziq-ovqat mahsulotlarini yaxshilash uchun konserva va oziq-ovqat konsentratlariga qo'shiladi.
Chipta raqami 16
Anilin - aminlarning vakili. Kimyoviy tuzilishi va xossalari, tayyorlanishi va amaliy qo'llanilishi.
Ominlar organik birikmalar, ular ammiakning hosilalari bo'lib, ularning molekulasida bir, ikki yoki uchta vodorod atomi uglevodorod radikali bilan almashtiriladi.
Umumiy formula:
Jismoniy xususiyatlar.
Anilin rangsiz yog'li suyuqlik bo'lib, zaif xarakterli hidga ega, suvda ozgina eriydi, lekin spirt, efir va benzolda eriydi. Qaynash nuqtasi 184 ° C. Anilin qonga ta'sir qiluvchi kuchli zahardir..
Kimyoviy xossalari.
Kislotalar (aminokislotalar bilan reaksiyalar)
Br 2 (suvli eritma)
C 6 H 5 NH 2 + HCl → C 6 H 5 NH 3 Cl
Anilinning kimyoviy xossalari uning molekulasida bir-biriga o'zaro ta'sir qiluvchi aminokislota - NH 2 va benzol halqasining mavjudligi bilan bog'liq.
Kvitansiya.
Nitro birikmalarining qaytarilishi - Zinin reaktsiyasi
C 6 H 5 NO 2 + H 2 → C 6 H 5 NH 2 + H 2 O
Ilova.
Anilin fotomateriallar va anilin bo'yoqlari ishlab chiqarishda qo'llaniladi. Polimerlar, portlovchi moddalar, dori vositalari olinadi.
Chipta raqami 17
Proteinlar biopolimerlarga o'xshaydi. Oqsillarning tuzilishi, xossalari va biologik funktsiyalari.
Sincaplar (oqsillar, polipeptidlar) - aminokislotalardan tashkil topgan yuqori molekulyar organik moddalar, zanjirda peptid bog'lari bilan bog'langan. Tirik organizmlarda oqsillarning aminokislotalar tarkibi aniqlanadi genetik kod, aksariyat hollarda sintez 20 ta standart aminokislotadan foydalanadi.
Protein tuzilishi
Protein molekulalari a-aminokislotalardan (monomerlar) va ba'zi hollarda modifikatsiyalangan asosiy aminokislotalardan tashkil topgan chiziqli polimerlardir. Proteindagi aminokislotalarning ketma-ketligi ushbu protein uchun gen tarkibidagi ma'lumotlarga mos keladi.
· Birlamchi tuzilish - polipeptid zanjiridagi aminokislotalarning ketma-ketligi - chiziqli.
· Ikkilamchi struktura polipeptid zanjirining vodorod bog'lari bilan mustahkamlangan spiralga aylanishidir.
· Uchinchi darajali struktura - ikkilamchi spiralni bobinga o'rash. Uchinchi darajali tuzilmani saqlang: disulfid aloqalari, vodorod aloqalari.
Xususiyatlari
Proteinlar aminokislotalar kabi amfoter moddalardir.
Ular suvda eruvchanlik darajasida farqlanadi, lekin ko'pchilik oqsillar unda eriydi.
Denaturatsiya: Proteinni kislota yoki gidroksidi bilan isitish yoki davolash kabi sharoitlarning keskin o'zgarishi oqsilning to'rtlamchi, uchinchi va ikkilamchi tuzilmalarini yo'qotishiga olib keladi. Denaturatsiya ba'zi hollarda qaytariladi.
Gidroliz: fermentlar ta'sirida oqsil uning tarkibidagi aminokislotalarga gidrolizlanadi. Bu jarayon, masalan, pepsin va tripsin kabi fermentlar ta'siri ostida inson oshqozonida sodir bo'ladi.
Oqsillarning organizmdagi vazifalari
Katalitik funktsiya
Fermentlar o'ziga xos katalitik xususiyatlarga ega bo'lgan oqsillar guruhidir. Fermentlar orasida quyidagi oqsillarni qayd etish mumkin: tripsin, pepsin, amilaza, lipaza.
Strukturaviy funktsiya
Proteinlar deyarli barcha to'qimalarning qurilish materialidir: mushak, qo'llab-quvvatlovchi, yaxlit.
Himoya funktsiyasi
Viruslar va patogen bakteriyalarni zararsizlantirishi mumkin bo'lgan antikor oqsillari .
Signal funktsiyasi
Retseptor oqsillari qo'shni hujayralardan olingan signallarni qabul qiladi va uzatadi.
Transport funktsiyasi
Gemoglobin kislorodni o'pkadan boshqa to'qimalarga va karbonat angidridni to'qimalardan o'pkaga olib boradi.
Saqlash funktsiyasi
Bu oqsillarga o'simlik urug'lari va hayvonlar tuxumlarida energiya va moddalar manbai sifatida saqlanadigan zahira oqsillari kiradi. Ular qurilish materiali sifatida xizmat qiladi.
Dvigatel funktsiyasi
Kontraktil faollikni amalga oshiradigan oqsillar aktin va miyozindir
18-raqamli chipta
1. umumiy xususiyatlar yuqori molekulyar birikmalar: tarkibi, tuzilishi, ularni ishlab chiqarishda yotuvchi reaktsiyalar (polietilen misolida).
Yuqori molekulyar birikmalar (polimerlar) makromolekulalari qayta-qayta takrorlanuvchi birliklardan tashkil topgan moddalardir. Ularning nisbiy molekulyar og'irligi bir necha mingdan ko'p milliongacha bo'lishi mumkin.
Monomer past molekulyar modda bo'lib, undan polimer olinadi.
Strukturaviy aloqa- polimer makromolekulasida ko'p marta takrorlangan atomlar guruhlari.
 Polimerlanish darajasi– takrorlanuvchi tuzilmaviy birliklar soni.
Polimerlanish darajasi– takrorlanuvchi tuzilmaviy birliklar soni.
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n
Polimerlarni polimerlanish va polikondensatsiya reaksiyalari orqali olish mumkin.
Reaktsiya belgilari polimerizatsiya:
1. Qo'shimcha mahsulotlar hosil bo'lmaydi.
2. Reaksiya ikki yoki uch bog'lanish tufayli sodir bo'ladi.
nCH 2 =CH 2 → (-CH 2 -CH 2 -) n– etilen polimerlanish reaksiyasi – polietilen hosil bo‘lishi.
Reaktsiya belgilari polikondensatsiya:
1. Qo'shimcha mahsulotlar hosil bo'ladi.
2. Reaksiya funksional guruhlar tufayli yuzaga keladi.
Misol: fenol va formaldegiddan fenol-formaldegid smolasining hosil bo'lishi, aminokislotalardan polipeptid bog'lanishi. Bunday holda, polimerga qo'shimcha ravishda, yon mahsulot - suv hosil bo'ladi.
Yuqori molekulyar birikmalar boshqa materiallarga nisbatan ma'lum afzalliklarga ega: ular reaktivlarga chidamli, tok o'tkazmaydi, mexanik jihatdan mustahkam va engil. Polimerlardan plyonkalar, laklar, kauchuk va plastmassalar tayyorlanadi.
Aminokislotalar, oqsillar va peptidlar quyida tavsiflangan birikmalarga misollardir. Ko'pgina biologik faol molekulalar bir-biri bilan va bir-birining funktsional guruhlari bilan o'zaro ta'sir qilishi mumkin bo'lgan kimyoviy jihatdan farq qiladigan bir nechta funktsional guruhlarni o'z ichiga oladi.
Aminokislotalar.
Aminokislotalar- karboksil guruhini o'z ichiga olgan organik bifunksional birikmalar - UNS, amino guruhi esa N.H. 2 .
Alohida α Va β - aminokislotalar:
Ko'pincha tabiatda uchraydi α - kislotalar. Proteinlar 19 ta aminokislota va bitta iminokislotadan iborat ( C 5 H 9YO'Q 2 ):


Eng oddiy aminokislota- glitsin. Qolgan aminokislotalarni quyidagi asosiy guruhlarga bo'lish mumkin:
1) glitsin gomologlari - alanin, valin, leysin, izolösin.
Aminokislotalarni olish.
Aminokislotalarning kimyoviy xossalari.
Aminokislotalar- bular amfoter birikmalar, chunki 2 ta qarama-qarshi funktsional guruh - aminokislota va gidroksil guruhini o'z ichiga oladi. Shuning uchun ular kislotalar va ishqorlar bilan reaksiyaga kirishadilar:
Kislota-asos almashinuvi quyidagicha ifodalanishi mumkin:
Aminokislotalarning xossalari ikki guruhga bo'lish mumkin: kimyoviy va fizik.
Aminokislotalarning kimyoviy xossalari
Aralashmalarga qarab aminokislotalar turli xossalarni namoyon qilishi mumkin.
Aminokislotalarning o'zaro ta'siri:
Aminokislotalar amfoter birikmalar sifatida ham kislotalar, ham ishqorlar bilan tuzlar hosil qiladi.
Karboksilik kislotalar sifatida aminokislotalar funktsional hosilalar hosil qiladi: tuzlar, efirlar, amidlar.
Aminokislotalarning o'zaro ta'siri va xossalari sabablari:
Tuzlar hosil bo'ladi:
NH 2 -CH 2 -COOH + NaOH NH 2 -CH 2 -COONa + H2O
Natriy tuzi + 2-amino sirka kislotasi Aminoasetik kislotaning natriy tuzi (glisin) + suv
Bilan o'zaro ta'sir qilish spirtli ichimliklar:
Aminokislotalar vodorod xlorid gazi ishtirokida spirtli ichimliklar bilan reaksiyaga kirishishi mumkin efir. Aminokislota efirlari bipolyar tuzilishga ega emas va uchuvchan birikmalardir.
NH 2 -CH 2 -COOH + CH 3 OH NH 2 -CH 2 -COOCH 3 + H 2 O.
Metil ester / 2-aminoasetik kislota /
O'zaro ta'sir ammiak:
Amidlar hosil bo'ladi:
NH 2 -CH(R)-COOH + H-NH 2 = NH 2 -CH(R)-CONH 2 + H 2 O
Aminokislotalarning o'zaro ta'siri kuchli kislotalar:
Biz tuzlarni olamiz:
HOOC-CH 2 -NH 2 + HCl → Cl (yoki HOOC-CH 2 -NH 2 * HCl)
Bu aminokislotalarning asosiy kimyoviy xossalari.
Aminokislotalarning fizik xossalari
Keling, aminokislotalarning fizik xususiyatlarini sanab o'tamiz:
- Rangsiz
- Kristalli shaklga ega bo'ling
- Ko'pgina aminokislotalar shirin ta'mga ega, ammo radikal (R) ga qarab, ular achchiq yoki ta'msiz bo'lishi mumkin
- Suvda oson eriydi, lekin ko'p organik erituvchilarda yomon eriydi
- Aminokislotalar optik faollik xususiyatiga ega
- 200 ° C dan yuqori haroratlarda parchalanish bilan eriydi
- O'zgaruvchan
- Aminokislotalarning kislotali va ishqoriy muhitdagi suvli eritmalari elektr tokini o'tkazadi









